甲狀腺癌診療規范(2018年版)
甲狀腺癌診療規范(2018年版)
一、概述
甲狀腺癌(Thyroid Cancer)是一種起源于甲狀腺濾泡上皮或濾泡旁上皮細胞的惡性腫瘤,也是頭頸部最為常見的惡性腫瘤。近年來,全球范圍內甲狀腺癌的發病率增長迅速,據全國腫瘤登記中心的數據顯示,我國城市地區女性甲狀腺癌發病率位居女性所有惡性腫瘤的第4位。我國甲狀腺癌將以每年20%的速度持續增長。
根據腫瘤起源及分化差異,甲狀腺癌又分為:甲狀腺乳頭狀癌(papillary thyroid carcinoma,PTC)、甲狀腺濾泡癌(follicular thyroid carcinoma,FTC)、甲狀腺髓樣癌(medullary thyroid carcinoma,MTC)以及甲狀腺未分化癌(anaplastic thyroid cancer,ATC),其中PTC最為常見,約占全部甲狀腺癌的85%~90%,而PTC和FTC合稱分化型甲狀腺癌(differentiated thyroid carcinoma,DTC)。不同病理類型的甲狀腺癌,在其發病機制、生物學行為、組織學形態、臨床表現、治療方法以及預后等方面均有明顯不同。DTC生物行為溫和,預后較好。ATC的惡性程度極高,中位生存時間僅7~10個月。MTC的預后居于兩者之間。
二、診療技術和應用
(一)高危人群的監測篩查
有如下病史時需要高度警惕甲狀腺癌,盡早進行篩查:①童年期頭頸部放射線照射史或放射性塵埃接觸史;②全身放射治療史;③DTC、MTC或多發性內分泌腺瘤病2型(MEN2型)、家族性多發性息肉病、某些甲狀腺癌綜合征[如多發性錯構瘤綜合征(multiple hamartoma syndrome)、Carney綜合征、沃納綜合征(Werner syndrome)和加德納綜合征(Gardner syndrome)]等的既往史或家族史。
(二)臨床表現
1.癥狀
大多數甲狀腺結節患者沒有臨床癥狀。通常在體檢時通過甲狀腺觸診和頸部超聲檢查而發現甲狀腺小腫塊。合并甲狀腺功能異常時可出現相應的臨床表現,如甲狀腺功能亢進或甲狀腺功能減退。晚期局部腫塊疼痛,可出現壓迫癥狀,常可壓迫氣管、食管,使氣管、食管移位。腫瘤局部侵犯重時可出現聲音嘶啞、吞咽困難或交感神經受壓引起霍納綜合征(Horner syndrome),侵犯頸叢可出現耳、枕、肩等處疼痛等癥狀。頸淋巴結轉移引起的頸部腫塊在未分化癌發生較早。髓樣癌由于腫瘤本身可產生降鈣素和5-羥色胺,可引起腹瀉、心悸、面色潮紅等癥狀。
2.體征
甲狀腺癌體征主要為甲狀腺腫大或結節,結節形狀不規則、與周圍組織粘連固定,并逐漸增大,質地硬,邊界不清,初起可隨吞咽運動上下移動,后期多不能移動。若伴頸部淋巴結轉移,可觸診頸部淋巴結腫大。
3.侵犯和轉移
(1)局部侵犯:甲狀腺癌局部可侵犯喉返神經、氣管、食管、環狀軟骨及喉,甚至可向椎前組織侵犯,向外側可侵犯至頸鞘內的頸內靜脈、迷走神經或頸總動脈。
(2)區域淋巴結轉移:PTC易早期發生區域淋巴轉移,大部分PTC患者在確診時已存在頸淋巴轉移。PTC淋巴結轉移常見原發灶同側、沿淋巴引流路徑逐站轉移,其淋巴引流一般首先至氣管旁淋巴結,然后引流至頸靜脈鏈淋巴結(Ⅱ~Ⅳ區)和頸后區淋巴結(Ⅴ區),或沿氣管旁向下至上縱隔(Ⅶ區)。Ⅵ區為最常見轉移部位,隨后依次為頸Ⅲ、Ⅳ、Ⅱ、Ⅴ區。同時,PTC淋巴結轉移以多區轉移為主,僅單區轉移較少見。Ⅰ區淋巴轉移少見(<3%)。少見的淋巴結轉移部位有咽后或咽旁淋巴結
(3)遠處轉移:肺部是甲狀腺癌常見的遠處轉移器官,甲狀腺癌也可出現骨轉移和顱內轉移。分化型甲狀腺癌較未分化甲狀腺癌或分化差的甲狀腺出現遠處器官轉移的可能性低。
4.常見并發癥
大部分的甲狀腺癌是分化型甲狀腺癌,生長相對較緩慢,極少引起并發癥。MTC因分泌降鈣素和5-羥色胺,可引起患者頑固性腹瀉,從而引起電解質紊亂。未分化癌生長迅速,可引起重度呼吸困難等并發癥。
(三)實驗室檢查
1.實驗室常規檢查
甲狀腺癌實驗室常規檢查的目的是了解患者的一般狀況以及是否適于采取相應的治療措施,包括血常規、肝腎功能等其他必要的實驗室檢查。如需進行有創檢查或手術治療的患者,還需要進行凝血功能等檢查。甲狀腺癌患者通常可伴有鈣、磷和鎂等離子的代謝異常,血清鈣磷鎂水平測定,有助于甲狀腺功能的評估。對需要將促甲狀腺激素(thyroid stimulating hormone,TSH)抑制到低于TSH正常參考范圍下限的DTC患者(特別是絕經后婦女),根據醫療條件酌情評估治療前基礎骨礦化狀態并定期監測;可選用血清鈣/磷、24小時尿鈣/磷、骨轉換生化標志物測定。
2.甲狀腺激素、甲狀腺自身抗體及腫瘤標志物檢查
(1)甲狀腺激素檢測:包括血液中四碘甲狀腺原氨酸(甲狀腺素,thyroxine,T4),三碘甲狀腺原氨酸(triiodothyronine,T3),游離T4(free thyroxine,FT4)和游離T3(free triiodothyronine,FT3)以及TSH的測定。TSH檢測是明確甲狀腺功能的重要初篩試驗,臨床普遍將TSH作為判斷甲狀腺功能紊亂的首要依據。所有甲狀腺結節患者,特別是甲狀腺癌高度疑似或確診患者均應檢測血清TSH水平。在需要應用甲狀腺核素顯像鑒別診斷甲狀腺結節良惡性時,血清TSH水平降低是重要的指征之一。在進行TSH抑制治療的甲狀腺癌患者中,也需要定期檢測血甲狀腺激素水平,并根據檢測結果調整左甲狀腺素(levo-thyroxine,L-T4),L-T4最終劑量的確定有賴于血清TSH的監測。
(2)甲狀腺自身抗體檢測:自身免疫性甲狀腺疾病相關的自身抗體主要有抗甲狀腺球蛋白抗體(anti-thyroglobulin antibodies,TgAb)、甲狀腺過氧化物酶抗體(thyroid peroxidase antibodies,TPOAb)和TSH受體抗體(thyrotropin receptor antibody,TRAb)。在DTC患者中,TgAb是血清甲狀腺球蛋白(thyroglobulin,Tg)的一個重要的輔助實驗。血清Tg水平還受到TgAb水平的影響,當TgAb存在時,會降低血清Tg的化學發光免疫分析方法檢測值,影響通過Tg監測病情的準確性;因此,每次測定血清Tg時均應同時檢測TgAb。甲狀腺過氧化物酶(thyroid peroxidase,TPO)是甲狀腺激素合成過程中的關鍵酶,TPOAb的出現通常早于甲狀腺功能紊亂,參與橋本甲狀腺炎和萎縮性甲狀腺炎發病中的組織破壞過程,引起臨床上甲狀腺功能減退癥狀。TRAb檢測結果陽性提示患者存在針對TSH受體的自身抗體。
(3)甲狀腺癌腫瘤標志物檢測:包括甲狀腺球蛋白(thyroglobulin,Tg),降鈣素(calcitonin,Ct)和癌胚抗原(carcinoembryonic antigen,CEA)。Tg是甲狀腺產生的特異性蛋白,但血清Tg測定對甲狀腺疾病病因診斷缺乏特異性價值。因此,臨床上一般不將血清Tg測定用于DTC的術前診斷。DTC患者治療后的隨訪階段,血清Tg變化是判別患者是否存在腫瘤殘留或復發的重要指標,可將血清Tg用于監測DTC術后的復發和轉移。還要根據DTC患者采取的手術方式和甲狀腺組織的保留情況進行綜合分析。對于已清除全部甲狀腺的DTC患者,只要出現血清Tg升高就提示有分化型甲狀腺癌復發或轉移的可能,提示進一步檢查。對于未完全切除甲狀腺的DTC患者,仍然建議術后定期(每6個月)測定血清Tg,術后血清Tg水平呈持續升高趨勢者,應考慮甲狀腺組織或腫瘤生長,需結合頸部超聲等其他檢查進一步評估。DTC隨訪中的血清Tg測定包括基礎Tg測定(TSH抑制狀態下)和TSH刺激后(TSH>30mU/L)的Tg測定。為更準確地反映病情,可通過停用L-T4或應用重組人促甲狀腺素(recombinant human thyrotropin,rhTSH)的方法,使血清TSH水平升高至>30mU/L,之后再行Tg檢測,即TSH刺激后的Tg測定。停用L-T4和使用rhTSH后測得的Tg水平具有高度一致性。復發危險度中、高危DTC患者,隨診復查時可選用TSH刺激后的Tg。
應注意,如果DTC細胞的分化程度低,不能合成和分泌Tg或產生的Tg有缺陷,也無法用Tg進行隨訪。對超聲難以確定良惡性的甲狀腺結節,可進行穿刺活檢,測定穿刺針沖洗液(包括囊實性結節的囊液)的Tg水平,可有助于提高確診率;對查體可觸及的以及超聲發現的可疑頸部淋巴結,淋巴結穿刺針沖洗液的Tg水平測定,可提高發現DTC轉移的敏感度。
MTC患者建議在治療前同時檢測血清Ct和CEA,并在治療后定期監測血清水平變化,如果超過正常范圍并持續增高,特別是當Ct≥150pg/ml時,應高度懷疑病情有進展或復發。血清Ct和CEA檢測,有助于髓樣癌患者的療效評估和病情監測。
(4)用于診斷的相關分子檢測:經FNAB仍不能確定良惡性的甲狀腺結節,可對穿刺標本進行某些甲狀腺癌的分子標記物檢測,如BRAF突變、Ras突變、RET/PTC重排等,有助于提高確診率。檢測術前穿刺標本的BRAF突變狀況,還有助于甲狀腺乳頭狀癌的診斷和臨床預后預測,便于制訂個體化的診治方案。
(四)超聲檢查
1.結節的良惡性鑒別
超聲檢查操作簡便、無創而廉價,高分辨率超聲可檢出甲狀腺內直徑>2mm的微小結節,清晰地顯示其邊界、形態及內部結構等信息,是甲狀腺最常用且首選的影像學檢查方法,推薦所有臨床觸診或機會性篩查等方式發現甲狀腺結節的患者均進行高分辨率頸部超聲檢查。頸部超聲檢查可證實甲狀腺結節存在與否,應確定甲狀腺結節的大小、數量、位置、囊實性、形狀、邊界、鈣化、血供及與周圍組織的關系,同時評估頸部有無異常淋巴結及其部位、大小、形態、血流和結構特點等。
甲狀腺結節惡性征象中特異性較高的為:微小鈣化、邊緣不規則、縱橫比>1;其他惡性征象包括:實性低回聲結節、暈圈缺如、甲狀腺外侵犯、伴有頸部淋巴結異常超聲征象等。頸部淋巴結異常征象主要包括:淋巴結內部出現微鈣化、囊性變、高回聲、周邊血流,此外還包括淋巴結呈圓形、邊界不規則或模糊、內部回聲不均、淋巴門消失或皮髓質分界不清等。
對甲狀腺結節及淋巴結的鑒別能力與超聲醫師的臨床經驗相關。甲狀腺影像報告和數據系統(TI-RADS)對甲狀腺結節惡性程度進行評估,有助于規范甲狀腺超聲報告,建議在有條件的情況下采用,但目前TI-RADS分類并未統一,可參考表1標準。超聲造影技術及超聲彈性成像可作為超聲診斷PTMC的補充手段,但不建議常規應用。
表1 TI-RADS分類
分類 | 評價 | 超聲表現 | 惡性風險 |
0 | 無結節 | 彌漫性病變 | 0 |
1 | 陰性 | 正常甲狀腺(或術后) | 0 |
2 | 良性 | 囊性或實性為主,形態規則、邊界清楚的良性結節 | 0 |
3 | 可能良性 | 不典型的良性結節 | <5% |
4 | 可疑惡性 | 惡性征象:實質性、低回聲或極低回聲、微小鈣化、邊界模糊/微分葉、縱橫比>1 | 5%~85% |
4a | 具有1種惡性征象 | 5%~10% | |
4b | 具有2種惡性征象 | 10~50% | |
4c | 具有3~4種惡性征象 | 50%~85% | |
5 | 惡性 | 超過4種惡性征象,尤其是有微鈣化和微分葉者 | 85%~100% |
6 | 惡性 | 經病理證實的惡性病變 |
2.超聲引導下細針穿刺活檢(US-FNAB)
FNAB利用細針對甲狀腺結節進行穿刺,從中獲取細胞成分,通過細胞學診斷對目標病灶性質進行判斷。US-FNAB可提高取材成功率和診斷準確率,同時有利于穿刺過程中對重要組織結構的保護及判斷穿刺后有無血腫,推薦作為進一步確定甲狀腺結節良惡性的診斷方法。
FNAB可分為細針抽吸活檢和無負壓細針活檢,臨床工作中可酌情選擇或聯合使用。為提高FNAB的準確性,可采取下列方法:在同一結節的多個部位重復穿刺取材;在超聲提示可疑征象的部分取材;在囊實性結節的實性部位取材,同時可進行囊液細胞學檢查。
(1)甲狀腺結節US-FNAB的適應證:直徑>1cm的甲狀腺結節,US有惡性征象者,推薦進行US-FNAB;直徑≤1cm的甲狀腺結節,不推薦常規行穿刺活檢,但若存在以下情況之一,可考慮超聲引導下FNAB:US提示甲狀腺結節有惡性征象;伴US所見頸部淋巴結異常;童年期有頸部放射線照射史或輻射污染接觸史;有甲狀腺癌家族史或甲狀腺癌綜合征病史;18F-FDG顯像陽性;伴血清降鈣素水平異常升高。
(2)US-FNAB的排除指征:經甲狀腺核素顯像證實為有自主攝取功能的熱結節;超聲檢查提示為純囊性的結節。
(3)甲狀腺結節US-FNAB的禁忌證:具有出血傾向,出、凝血時間顯著延長,凝血酶原活動度明顯減低;穿刺針途徑可能損傷鄰近重要器官;長期服用抗凝藥;頻繁咳嗽、吞咽等難以配合者;拒絕有創檢查者;穿刺部位感染,須處理后方可穿刺;女性行經期為相對禁忌證。
3.隨訪中的超聲檢查
對于未行手術治療的患者超聲隨訪中應注意原結節體積是否增大或出現前述惡性征象。結節體積增大指結節體積增大50%以上或至少有2條徑線增加超過20%(且超過2mm),此時有FNAB的適應證;對于囊實性結節,應根據實性部分的生長情況決定是否進行FNAB。
對于甲狀腺術后患者隨訪中應注意掃查術床區是否存在實性占位及頸部淋巴結是否有惡性表現。超聲對術床良性病變和復發病灶鑒別困難,對頸部淋巴結的評價同術前。術后可疑頸部淋巴結的穿刺指證:對于最小徑>8mm且超聲提示異常的淋巴結應行細針穿刺物洗脫液檢查(FNA-Tg);對于<8mm的淋巴結在沒有增長或威脅到周圍重要結構時可以不進行FNA或其他干預。
(五)影像學檢查
1.電子計算機斷層成像(CT)
正常甲狀腺含碘量高,與周圍組織密度明顯不同,CT平掃即可清楚顯示甲狀腺,注射對比劑后,對比度更加良好。CT掃描對評價甲狀腺腫瘤的范圍、與周圍重要結構如氣管、食管、頸動脈的關系及有無淋巴結轉移有重要價值。由于甲狀腺病變可侵入上縱隔或出現縱隔淋巴結腫大,故掃描范圍應常規包括上縱隔。CT對中央組淋巴結、上縱隔組淋巴結和咽后組淋巴結觀察具有優勢,并可對胸骨后甲狀腺病變、較大病變及其與周圍結構的關系進行觀察,可清晰顯示各種形態大小的鈣化灶,但對于最大徑≤5mm結節及彌漫性病變合并結節的患者觀察欠佳。對于甲狀腺再次手術的病例,了解殘留甲狀腺、評估病變與周圍組織的關系及評價甲狀腺局部及頸部的復發很有幫助。如無碘對比劑使用禁忌證,對于甲狀腺病變應常規行增強掃描。薄層圖像可以顯示較小的病灶和清晰顯示病變與周圍組織、器官的關系。
2.磁共振成像(MRI)
組織分辨率高,可以多方位、多參數成像,可評價病變范圍及與周圍重要結構的關系。通過動態增強掃描、DWI等功能成像可對結節良、惡性進行評估。其不足在于對鈣化不敏感,檢查時間長,易受呼吸和吞咽動作影響,故甲狀腺MRI檢查不如超聲及CT檢查普及,目前在甲狀腺的影像檢查方面應用不多。
3.正電子發射計算機斷層成像(PET-CT)
不推薦作為甲狀腺癌診斷的常規檢查方法,對于下列情況,有條件者可考慮使用:①DTC患者隨訪中出現Tg升高(>10ng/ml),且131I診斷性全身顯像(Dx-WBS)陰性者查找轉移灶;②MTC療前分期以及術后出現降鈣素升高時查找轉移灶;③甲狀腺未分化癌療前分期和術后隨訪;④侵襲性或轉移性DTC患者進行131I治療前評估(表現為PET-CT代謝增高的病灶攝取碘能力差,難以從131I治療中獲益)。
4.甲狀腺癌功能代謝顯像
甲狀腺癌功能代謝顯像原理是利用甲狀腺癌細胞對一些放射性顯像藥具有特殊的攝取濃聚機制,將這些顯像物引入體內后可被甲狀腺癌組織攝取和濃聚,應用顯像儀器如SPECT或SPECT-CT、PET-CT進行掃描,獲取病灶位置、形態、數量及代謝等信息進行定位、定性、定量分析。
在進行131I治療分化型甲狀腺癌(DTC)之前,通常需要明確DTC患者術后殘留甲狀腺的大小和功能情況,一般會進行甲狀腺顯像。甲狀腺顯像原理是正常甲狀腺組織具有選擇性攝取和濃聚碘的能力,锝與碘屬于同族元素,也能被甲狀腺組織攝取和濃聚,只是99mTcO4-進入甲狀腺細胞后不能進一步參加甲狀腺激素合成。99mTcO4-物理半衰期短,發射140keV的γ射線,能量適中,甲狀腺受輻射劑量小等,目前臨床上多使用99mTcO4-進行甲狀腺顯像。
(六)聲帶功能評估
1.術前評估
甲狀腺癌患者術前因常規進行間接喉鏡檢查,評估雙側聲帶活動情況,若出現聲帶活動減弱甚至固定的征象,應高度懷疑腫瘤壓迫或侵犯喉返神經,在術前做好相應的手術預案,并和患者充分溝通,告知有術后氣管切開或氣管造瘺的風險。如果術前間接喉鏡檢查不滿意,可進行術前電子纖維喉鏡或纖維支氣管鏡檢查,評估雙側聲帶活動情況。此外,對于臨床或影像學檢查(如頸部CT)懷疑腫瘤緊鄰或侵犯氣管的患者,應進行術前纖維支氣管鏡檢查,評估腫瘤是否侵透氣管全層至氣管腔內,以及侵犯范圍大小,是否影響麻醉氣管插管等,據此來制訂相應的手術方案和麻醉方案。
2.術后評估
術中發現腫瘤侵犯喉返神經,或術中喉返神經檢測提示喉返神經功能受影響,術后可行纖維電子喉鏡評估聲帶運動恢復情況。因雙側喉返神經受侵犯而進行的術中氣管造瘺或術后氣管切開的患者,可進行喉鏡的評估聲帶活動情況,決定拔除氣管套管或進行氣管造瘺修補的時機。
(七)甲狀腺癌細胞病理診斷規范
甲狀腺癌的細胞病理診斷規范由甲狀腺細針穿刺(fine needle aspiration,FNA)的取材、制片和診斷報告等部分組成。
1.FNA的取材
甲狀腺FNA的取材方法有觸診引導的FAN和超聲引導的FNA兩種。觸診引導的FNA僅適用于可觸及的實性結節;對于不可觸及的結節,囊實性結節或先前有過不滿意的FNA的結節均應行超聲引導下FNA。甲狀腺FNA常用穿刺針的外徑為22G~27G,對于纖維化明顯的病灶可選擇較粗的穿刺針,而對于血供豐富者可選較細的穿刺針。FNA操作時可以給少量負壓或無負壓運針,運針應多角度、快速進行。每個結節的進針次數1~3次,視針吸物的量而定。對于囊實性結節應有針對性的取實性區。
2.FNA的制片
細胞標本的制片技術包括常規涂片、液基制片和細胞塊切片。常規涂片是最常用的制片方法,穿出的細胞直接涂在玻片上,潮干,酒精固定。如果穿出物為囊性液體,液基制片的方法會使囊液中的細胞富集,從而獲得一張較常規涂片細胞量更為豐富的涂片。對于臨床懷疑是甲狀腺少見類型的腫瘤,如髓樣癌、未分化癌、轉移性癌等最好加做細胞塊,以便于行免疫細胞化學檢測。常規涂片與液基制片聯合應用可提高診斷的準確性,有條件的單位還可開展細胞標本的現場評估,以提高取材的滿意率。
3.細胞病理學診斷報告
細胞病理學診斷報告采用TBSRTC(The Bethesda System for Reporting Thyroid Cytopathology)報告系統,在此報告系統中,細胞學診斷分為六級:I級,不能診斷/不滿意;Ⅱ級,良性;Ⅲ級,意義不明的非典型細胞/意義不明的濾泡性病變;Ⅳ級,濾泡性腫瘤/可疑濾泡性腫瘤;Ⅴ級,可疑惡性和Ⅵ級,惡性(表2)。不同細胞學診斷分級的患者其惡性風險不同,臨床管理措施也不同(表3)。
表2 甲狀腺TBSRTC報告系統
Ⅰ 不能診斷/不滿意 |
囊液標本 |
上皮細胞量少 |
其他(如血多遮擋細胞、細胞過度干燥等) |
Ⅱ 良性 |
符合良性濾泡結節(包括腺瘤樣結節和膠質結節等) |
符合橋本甲狀腺炎 |
符合亞急性甲狀腺炎 |
Ⅲ 意義不明的非典型細胞/意義不明的濾泡性病變 |
Ⅳ 濾泡性腫瘤/可疑濾泡性腫瘤 |
如果是嗜酸細胞腫瘤,則請注明 |
Ⅴ 可疑惡性 |
可疑甲狀腺乳頭狀癌 |
可疑甲狀腺髓樣癌 |
可疑轉移性癌 |
可疑淋巴瘤 |
Ⅵ 惡性 |
甲狀腺乳頭狀癌 |
甲狀腺低分化癌 |
甲狀腺髓樣癌 |
甲狀腺未分化癌 |
鱗狀細胞癌 |
混合成分的癌(注明具體成分) |
轉移性惡性腫瘤 |
非霍奇金淋巴瘤 |
其他 |
表3 甲狀腺TBSRTC各診斷分級的惡性風險及臨床管理
診斷分級 | 惡性風險 | 臨床管理 |
不能診斷/不滿意 | 5%~10% | 重復FNA(超聲引導下) |
良性 | 0~3% | 隨診 |
意義不明的非典型細胞/意義不明的濾泡性病變 | 10%~30% | 重復FNA/分子檢測/手術 |
濾泡性腫瘤/可疑濾泡性腫瘤 | 25%~40% | 分子檢測/手術 |
可疑惡性 | 50%~75% | 手術 |
惡性 | 97%~99% | 手術 |
(八)甲狀腺癌組織病理診斷規范
1.重要性及目的
不同的甲狀腺腫瘤病理類型,其生物學行為也會區別較大,從良性的甲狀腺腺瘤、交界性甲狀腺濾泡性腫瘤到甲狀腺癌,對患者的預后、治療都會有很重要的影響,甲狀腺癌的淋巴結轉移情況同樣對患者治療策略具有重要意義。為了更好地為臨床醫師提供為患者制訂更加精準的隨診、治療方案的依據,讓不同級別的醫院、不同的病理醫師能夠站在相同的平臺進行患者診治的交流,規范的甲狀腺組織病理診斷十分重要。
2.術前穿刺病理診斷
術前超聲定位粗針穿刺,可以收集腫瘤組織送檢組織病理學診斷,在標本充足,形態典型的情況下可以明確診斷。由于FNA在甲狀腺癌診斷中具有明顯優勢,組織學穿刺一般不作為常規,在部分可疑少見類型的病例可作為補充使用。
3.術中冰凍病理診斷
目的是對術前未做穿刺病理診斷或病理診斷不明確的甲狀腺結節定性,對淋巴結有無轉移進行明確,以決定甲狀腺切除的術式或淋巴結清掃的范圍。
送檢冰凍注意事項如下。
甲狀腺:
(1)標本離體后不加任何固定液盡快送往病理科。
(2)如果腫瘤結節<5mm,在腫瘤處做標記(如切開或系縫線)。
(3)甲狀腺交界性腫瘤、甲狀腺濾泡癌的診斷需術后對標本進行整體觀察,充分取材后確診。
(4)冰凍石蠟不符情況需在術前或冰凍前作為知情同意告知患者及家屬,并簽字。
淋巴結:
(1)單獨送檢,以增加送檢分區的目的性和病理診斷的準確性,避免漏診。
(2)離體后盡快送檢,保持標本新鮮,放至透明塑料小袋或標本盒中,做好密封,送至病理科。
(3)過小標本不能在體外放置過久,避免干硬,造成無法冰凍制片或顯微鏡下無法準確觀察。
(4)如果病理顯微鏡下發現淋巴結內有砂粒體,應該進行連續切片,尋找有無轉移的證據。
(5)淋巴結術中冰凍陰性,而術后石蠟深切出現轉移癌的情況并不少見,需在術前或冰凍前作為知情同意告知患者及家屬,并簽字。
4.術后石蠟病理診斷
取材注意事項
(1)垂直于長軸行2~3mm平行切開。
(2)仔細檢查,注意微小癌或結節。
(3)對多發病灶,如懷疑惡性,每個病灶均應取材。
(4)懷疑為包膜內或微小侵襲性濾泡癌病例,腫瘤結節被膜全部取材。
(5)注意腫物與被膜的關系。
(6)注意檢查甲狀腺周圍組織(帶狀肌、淋巴結或甲狀旁腺)。
診斷規范:即病理報告中應包含的內容。
(1)病理類型、亞型、病灶數目。
(2)纖維化及鈣化情況。
(3)有無脈管及神經侵犯(近被膜處小神經侵犯還是喉返神經分支)。
(4)甲狀腺被膜受累情況。
(5)帶狀肌侵犯情況。
(6)周圍甲狀腺有無慢性淋巴細胞性甲狀腺炎、結節性甲狀腺腫、腺瘤樣改變等。
(7)淋巴結轉移情況+淋巴結被膜外受侵情況。
(8)pTNM分期(AJCC第8版)。
(9)必要的免疫組化。
(九)鑒別診斷
1.甲狀腺腺瘤:本病多見于20~30歲年輕人,多為單結節,邊界清,表面光滑,生長緩慢,突然增大常為囊內出血,無頸淋巴結轉移和遠處轉移。
2.結節性甲狀腺腫:多見于中年以上婦女,病變可長達數年至數十年,常累及雙側甲狀腺,為多結節,大小不一,病程長者可有囊性變,腫物巨大可出現壓迫氣管,使氣管移位,并有不同程度的呼吸困難的表現;當腫瘤壓迫食管,會出現吞咽困難的表現。可發生癌變,腫物增大明顯加快。
3.亞急性甲狀腺炎:常認為是由病毒感染引起,病期數周或數月,發病前常有呼吸道感染的病史,可伴有輕度發熱,局部有疼痛,以吞咽時明顯,可放射到耳部,甲狀腺彌漫性增大,也可出現不對稱的結節樣腫物,腫物有壓痛。本病為自限性疾病,約經數周的病程可自愈。少數患者需手術以排除甲狀腺癌。
4.慢性淋巴細胞性甲狀腺炎(又稱橋本甲狀腺炎):為慢性進行性雙側甲狀腺腫大,有時與甲狀腺癌難以區別,一般無自覺癥狀,自身抗體滴度升高。本病對腎上腺皮質激素較敏感,有時需要手術治療,少量X線治療效果好。
5.纖維性甲狀腺炎:甲狀腺普遍增大,質硬如木,但常保持甲狀腺原來的外形。常與周圍組織固定并產生壓迫癥狀,常與癌難以鑒別。可手術探查,并切除峽部,以緩解或預防壓迫癥狀。
三、甲狀腺癌的診斷:分類和分期
(一)甲狀腺癌的組織學分類
根據世界衛生組織(World Health Organization,WHO)的定義,甲狀腺腫瘤的組織學分類主要分為:原發性上皮腫瘤、原發性非上皮腫瘤與繼發性腫瘤。
甲狀腺腫瘤的分類
I.原發性上皮腫瘤
A.濾泡上皮腫瘤
良性:濾泡性腺瘤。
惡性:甲狀腺癌。①分化型甲狀腺癌:乳頭狀癌(PTC)、濾泡狀癌(FTC)、分化差癌;②未分化癌(ATC)。
B.C細胞腫瘤(MTC)
C.濾泡上皮與C細胞混合性腫瘤
Ⅱ.原發性非上皮腫瘤
A.惡性淋巴瘤
B.肉瘤
C.其他
Ⅲ.繼發性腫瘤
約95%的甲狀腺腫瘤來源于甲狀腺濾泡細胞,其余的多來源于C細胞(甲狀腺濾泡旁細胞)。濾泡上皮與C細胞混合性腫瘤十分罕見,同時含有濾泡上皮來源與C細胞來源的腫瘤細胞,其在組織來源上是否作為一種獨立的甲狀腺腫瘤尚有爭議。甲狀腺惡性淋巴瘤是最常見的甲狀腺非上皮來源腫瘤,可獨立發生于甲狀腺,亦可為全身淋巴系統腫瘤的一部分。甲狀腺肉瘤、繼發性甲狀腺惡性腫瘤等在臨床中較少見,多為零星個案報道。
1.PTC及其亞型
PTC亞型近年來較多被關注,最常見的是經典型和濾泡亞型。經典型約占PTC50%左右,主要形態特征是乳頭結構和核型改變,核分裂象罕見,砂礫樣鈣化較為常見,主要位于淋巴管或間質。文獻報道20%~40%的病例會出現鱗狀化生。常見淋巴管侵犯,血管侵犯不常見,但也可出現。免疫表型:乳頭狀癌TG、TTF1、PAX8及廣譜CK陽性;CK20、CT及神經內分泌標記通常陰性。濾泡亞型主要以濾泡性生長方式為主,具有經典型PTC的核型。發生率占PTC的40%左右。
PTC其他常見亞型包括彌漫硬化性、高細胞亞型和柱狀細胞亞型等,一般認為預后較經典型和濾泡亞型差。
(1)彌漫硬化型:多見于年輕女性患者,雙側或單側甲狀腺腺葉彌漫性增大受累,具有自身免疫性甲狀腺炎的血清學特點。形態學特點見顯著硬化,大量砂礫體,慢性淋巴細胞性甲狀腺炎背景,腫瘤細胞巢常呈實性,伴廣泛鱗狀化生,容易侵犯甲狀腺內淋巴管及甲狀腺外組織。RET重排常見,而BARF突變罕見。約10%~15%的病例發生遠處轉移,最常見轉移至肺。
(2)高細胞亞型:主要組成細胞的高度是寬度的2~3倍,有豐富的嗜酸性胞質,具有經典型的核型特點。高細胞區域至少占30%。常見于年齡較大患者,侵襲性比經典型強,更容易發生甲狀腺外侵犯及遠處轉移。大多數病例有BRAF突變(60%~95%)。
(3)柱狀細胞亞型:這種罕見亞型由假復層柱狀細胞構成,缺乏經典型乳頭狀癌的核型。腫瘤細胞偶可顯示核下空泡及透明胞質,類似于子宮內膜癌或腸型腺癌。免疫染色CDX2通常陽性。TTF1不同程度陽性。
(4)篩狀-桑葚樣亞型:這種亞型被認為是甲狀腺癌的一種獨特亞型,可出現在散發性病例,也可以出現在家族性腺瘤性息肉病,幾乎總是發生在女性。散發性病例通常為單灶,而家族性常為多灶。腫瘤通常是包膜內病變,具有篩狀、濾泡、乳頭、梁狀、實性及桑葚樣結構等混合的生長方式。包膜/血管侵犯常見。乳頭通常被覆柱狀形態的細胞,缺乏腔內膠質。核并非特別透明。免疫染色TTF1常斑駁陽性。TG局灶或弱陽性。B-catenin顯示特征性核陽性。
2.FTC及其亞型
FTC是甲狀腺濾泡細胞來源的惡性腫瘤,缺乏乳頭狀癌核型特征,有包膜或浸潤性生長方式。發病率6%~10%。包含亞型:①濾泡癌,微小浸潤型(僅包膜侵犯);②濾泡癌,包膜內血管浸潤型;③濾泡癌,廣泛浸潤型。FTC淋巴結轉移較PTC少見而易發生遠處轉移。
Hürthle(嗜酸性)細胞腫瘤是一類通常有包膜的嗜酸細胞組成腫瘤,濾泡細胞來源,可歸為FTC或獨立成為一種類型,較為罕見。分為:Hürthle(嗜酸)細胞腺瘤和Hürthle(嗜酸)細胞癌。
具有乳頭狀核特征的非浸潤性濾泡性腫瘤(Non-invasivefollicularthyroidneoplasmwithpapillary-likenuclearfeatures,NIFTP)是一類界清或有包膜的、濾泡型生長方式的非浸潤性腫瘤,腫瘤細胞具有乳頭狀癌核特征。
3.MTC及其亞型
MTC是甲狀腺C細胞(濾泡旁細胞)來源的惡性腫瘤。發病率2%~3%,分為散發性和家族性,散發性約占全部髓樣癌的70%,好發于50~60歲,家族性發病年齡輕,約占30%,是常染色體顯性遺傳疾病。多發性神經內分泌腫瘤(multipleendocrineneoplasia,MEN)2型,包括2A、2B和家族性髓樣癌,目前家族性髓樣癌被認為是MEN2A的疾病譜。
血清降鈣素的水平與腫瘤負荷相關,但也有<1%的病例為非分泌性的。血清CEA的檢查是髓樣癌隨診過程中的重要指標,尤其是在降鈣素低水平時,更有意義。
髓樣癌的鏡下特征多樣,可以與甲狀腺任意惡性腫瘤相似,典型結構為實性、分葉、管狀或島狀。腫瘤細胞體積變化較大,可以是圓形、多角形、漿細胞樣或梭形。細胞核低-中度異型,核分裂活性相對較低。
亞型:根據細胞和結構特征分為不同類型,乳頭型/假乳頭型、濾泡型(管狀/腺樣)、梭形細胞型、巨細胞型、透明細胞型、嗜酸細胞型、黑色素型、鱗狀亞型、副節瘤樣型、血管肉瘤樣型、小細胞型、包膜內甲狀腺髓樣癌等。
免疫組化指標:髓樣癌可以表達:降鈣素、神經內分泌標記物(CD56、突觸素、嗜鉻素A)、TTF-1、PAX8和CEA等。不表達TG。
4.甲狀腺低分化癌和ATC
甲狀腺低分化癌是顯示有限的濾泡細胞分化的甲狀腺濾泡性腫瘤,在形態和生物學行為上介于分化型甲狀腺癌(甲狀腺乳頭狀癌及濾泡癌)和未分化型甲狀腺癌之間。主要的組織學形態有島狀、梁狀和實性,核分裂象易見,大片壞死可導致殘留腫瘤細胞呈血管外皮瘤樣聚集在血管周圍,甲狀腺低分化癌可以同時伴有不同比例的分化型癌成分,但有研究顯示即使出現10%的甲狀腺低分化癌成分也伴隨著侵襲性行為和對預后的不良影響。甲狀腺低分化癌的Ki-67指數通常在10-30%,BCL2、CyclinD1通常陽性,P53、P21和P27灶狀陽性。鑒別診斷主要包括原發甲狀腺髓樣癌、甲狀旁腺癌和轉移到甲狀腺的癌。
ATC是由未分化的甲狀腺濾泡細胞構成的高度侵襲性惡性腫瘤。患者典型癥狀為迅速增大、質硬、固定的頸部包塊伴廣泛侵犯周圍組織,大約30%~40%患者伴有遠處轉移如肺、骨和腦。主要的組織學形態有肉瘤樣、瘤巨細胞樣和上皮樣,以上形態可單獨或不同比例混合出現,也可以出現灶狀的鱗狀分化或異源性分化;通常伴有壞死、多量的核分裂象和血管侵犯。免疫組化:TTF1和TG通常陰性,PAX8大概一半病例陽性,CK可以在上皮樣分化區域陽性,LCA、肌源性標記和黑色素瘤標記等主要用于排除性診斷。鑒別診斷:其他類型高度惡性腫瘤如肌源性肉瘤、惡性黑色素瘤和大細胞淋巴瘤等。非濾泡和濾泡旁細胞來源的高度惡性的甲狀腺原發腫瘤一般也歸為ATC范疇,例如鱗狀細胞癌、肉瘤、黏液表皮樣癌等。
(二)甲狀腺癌的分期
1.AJCC分期
針對甲狀腺癌的分期包括根據術前評估(病史、查體、輔助檢查)確立的臨床分期(cTNM)和根據術后病理的病理分期(pTNM),具體分期標準如下(AJCC第8版)。
甲狀腺乳頭狀癌、濾泡癌、低分化癌、Hürthle細胞癌和未分化癌
pTX:原發腫瘤不能評估
pT0:無腫瘤證據
pT1:腫瘤局限在甲狀腺內,最大徑≤2cm
T1a腫瘤最大徑≤1cm
T1b腫瘤最大徑>1cm,≤2cm
pT2:腫瘤2~4cm
pT3:腫瘤>4cm,局限于甲狀腺內或大體侵犯甲狀腺外帶狀肌
pT3a:腫瘤>4cm,局限于甲狀腺內
pT3b:大體侵犯甲狀腺外帶狀肌,無論腫瘤大小
帶狀肌包括:胸骨舌骨肌、胸骨甲狀肌、甲狀舌骨肌、肩胛舌骨肌
pT4:大體侵犯甲狀腺外帶狀肌外
pT4a:侵犯喉、氣管、食管、喉反神經及皮下軟組織
pT4b:侵犯椎前筋膜,或包裹頸動脈、縱隔血管
甲狀腺髓樣癌
pTX:原發腫瘤不能評估
pT0:無腫瘤證據
pT1:腫瘤局限在甲狀腺內,最大徑≤2cm
T1a腫瘤最大徑≤1cm
T1b腫瘤最大徑>1cm,≤2cm
pT2:腫瘤2~4cm
pT3:腫瘤>4cm,局限于甲狀腺內或大體侵犯甲狀腺外帶狀肌
pT3a:腫瘤>4cm,局限于甲狀腺內
pT3b:大體侵犯甲狀腺外帶狀肌,無論腫瘤大小
帶狀肌包括:胸骨舌骨肌、胸骨甲狀肌、甲狀舌骨肌、肩胛舌骨肌
pT4:進展期病變
pT4a:中度進展,任何大小的腫瘤,侵犯甲狀腺外頸部周圍器官和軟組織,如喉、氣管、食管、喉反神經及皮下軟組織
pT4b:重度進展,任何大小的腫瘤,侵犯椎前筋膜,或包裹頸動脈、縱隔血管
區域淋巴結:適用于所有甲狀腺癌
pN0:無淋巴結轉移證據
pN1:區域淋巴結轉移
pN1a:轉移至Ⅵ、Ⅶ區(包括氣管旁、氣管前、喉前/Delphian或上縱隔)淋巴結,可以為單側或雙側。
pN1b:單側、雙側或對側頸淋巴結轉移(包括Ⅰ、Ⅱ、Ⅲ、Ⅳ或Ⅴ區)淋巴結或咽后淋巴結轉移。
乳頭狀或濾泡狀癌(分化型) | |||
年齡<55歲 | |||
T | N | M | |
Ⅰ期 | 任何 | 任何 | 0 |
Ⅱ期 | 任何 | 任何 | 1 |
年齡≥55歲 | |||
Ⅰ期 | 1 | 0/x | 0 |
2 | 0/x | 0 | |
Ⅱ期 | 1~2 | 1 | 0 |
3a~3b | 任何 | 0 | |
Ⅲ期 | 4a | 任何 | 0 |
ⅣA期 | 4b | 任何 | 0 |
ⅣB期 | 任何 | 任何 | 1 |
髓樣癌(所有年齡組) | |||
Ⅰ期 | 1 | 0 | 0 |
Ⅱ期 | 2~3 | 0 | 0 |
Ⅲ期 | 1~3 | 1a | 0 |
ⅣA | 4a | 任何 | 0 |
1~3 | 1b | 0 | |
ⅣB期 | 4b | 任何 | 0 |
ⅣC期 | 任何 | 任何 | 1 |
未分化癌(所有年齡組) | |||
ⅣA期 | 1~3a | 0/x | 0 |
ⅣB期 | 1~3a | 1 | 0 |
3b~4 | 任何 | 0 | |
ⅣC期 | 任何 | 任何 | 1 |
2.甲狀腺癌的預后相關因素
某種特定的腫瘤特點將影響腫瘤預后。可能最重要的因素是腫瘤的組織類型,原發腫瘤大小,局部浸潤,壞死,血管浸潤,BRAF突變,遠處轉移。
(1)組織類型
雖然典型乳頭狀癌患者的生存率很好,但腫瘤死亡率在特定的分化子類型之間有很大差別。分化好的腫瘤有包膜,約占乳頭癌的10%,是良好預后的表現。預后不好與下面因素有關:①高細胞乳頭狀癌亞型,10年死亡率達25%。②柱狀細胞乳頭狀癌亞型,增長迅速,死亡率高。③彌漫性硬化性亞型,整個甲狀腺浸潤。濾泡樣變異性乳頭狀癌,特征是具有濾泡樣結構、典型的乳頭狀細胞,在有包膜的情況下比起一般乳頭狀癌沒有顯示更壞的預后。
濾泡狀癌的典型特征是有包膜的孤立腫瘤,比乳頭狀癌更富有侵襲性。濾泡狀癌通常有微濾泡結構,由于濾泡細胞浸潤至包膜或血管而診斷為癌,浸潤至血管者預后比浸潤包膜者更差。大多數濾泡狀癌侵襲性小,一般只輕度穿破包膜而不發生血管轉移,這些病變與濾泡腺癌相似,發生遠處轉移或致死的可能性較小。通過FNA或冰凍切片無法鑒別濾泡腺瘤和低侵襲性濾泡狀甲狀腺癌,只能通過永久組織切片,看到濾泡細胞浸潤包膜才能確診。高侵襲性濾泡狀甲狀腺癌不是很常見,又是會在手術中發現其侵襲周圍組織及血管。80%的高侵襲性的濾泡狀甲狀腺癌發生轉移,導致20%的患者在被診斷后幾年內死亡。預后差與診斷時患者年齡大,腫瘤分期高,腫瘤體積大密切相關。
乳頭癌與濾泡癌預后相似,如果腫瘤局限于甲狀腺內,直徑小于1.0cm,或微轉移兩者都有較好的預后。如果出現遠處轉移,高侵襲,則預后差。
(2)原發腫瘤大小
乳頭狀癌<1cm,命名為微小癌,通常為體檢發現,致死率幾乎為0。
另外一些生物學行為較差小乳頭癌的臨床表現不同。例如,約20%的多發微小癌出現頸淋巴結轉移;一些研究發現近60%的頸淋巴結轉移來自多發的微小癌,這種腫瘤更可能出現遠處轉移。
腫瘤<1.5cm乳頭癌或濾泡癌發現遠處轉移可能性較小,而較大腫瘤30年內復發率為33%。<1.5cm乳頭癌或濾泡癌30年死亡率為0.4%,而較大腫瘤(>1.5cm)為7%(P<0.01)。實事上腫瘤大小與預后、死亡率呈線性關系。
(3)局部侵犯
10%的分化甲狀腺癌出現局部侵犯,造成局部器官功能不全,增加死亡率。局部入侵的腫瘤局部復發是沒有入侵的2倍,33%有局部入侵的患者死亡。
(4)淋巴結轉移
區域淋巴轉移對預后作用有爭議。一些學者認為發現區域淋巴結轉移不影響復發和生存率。另外一些學者認為淋巴結轉移是局部復發和癌相關死亡率的高危因素之一。淋巴轉移與遠處轉移有一定相關性,尤其是那些雙側頸淋巴結轉移,或穿破淋巴結包膜,或縱隔淋巴結轉移。
(5)遠處轉移
對于乳頭狀癌和濾泡型癌來說遠處轉移是引起致死的主要原因。10%的乳頭狀癌、25%的濾泡型癌會出現遠處轉移,近50%的病例在診斷時即有遠處轉移。遠處轉移在霍斯勒細胞癌和年齡>40歲的患者中發現率更高(35%)。遠處轉移位置:在13個研究中報道的1231名出現遠處轉移的患者當中,肺轉移(49%)、骨轉移(25%)、肺和骨轉移(15%)、中樞神經系統(CNS)或其他軟組織轉移(10%)。大病灶肺轉移不濃聚131I和小結節轉移在X線上可以發現,而131I不濃聚者預后差。
3.分化型甲狀腺癌的復發風險分層
DTC疾病復發率風險分級系統,其根據術中病理特征如病灶殘留、腫瘤大小與數目、病理亞型、包膜血管侵犯、淋巴結轉移與外侵、術后刺激性Tg水平、分子病理特征等因素將患者復發風險分為低、中、高危3層(表4)。對于高危組DTC強烈建議術后行輔助治療;中危組可行輔助治療;低危組一般不行清甲治療,但須行內分泌治療。
表4 DTC復發風險分層
危險分層 臨床病理特征
低危 甲狀腺乳頭狀癌(包括以下所有)
無區域淋巴結或遠處轉移
大體腫瘤無殘留
腫瘤無外侵
非惡性程度高的組織學亞型
首次術后全身核素掃描未見甲狀腺床外的攝碘灶
無血管侵犯
cN0或少于5個微小淋巴結轉移(直徑<0.2cm)
濾泡狀亞型乳頭狀癌,位于甲狀腺內,未突破包膜;甲狀腺乳頭狀微小癌,位于甲狀腺內,單發或多發,包括BRAFV600E突變
濾泡性甲狀腺癌,位于甲狀腺內,分化好,有包膜侵犯且無血管侵犯,或僅有微小血管侵犯
中危 甲狀腺周圍組織的微小侵犯
術后首次核素顯像有頸部病灶攝碘
惡性程度高的亞型(高細胞、柱狀細胞、彌漫硬化等)
伴有血管侵犯,cN1或5個以上淋巴結轉移的pN1,轉移淋巴結直徑小于3cm
多灶性甲狀腺乳頭狀微小癌伴或不伴BRAFV600E突變
高危 明顯侵犯甲狀腺周圍軟組織
腫瘤殘留
遠處轉移
術后血清Tg提示遠處轉移
pN1且轉移淋巴結大于3cm
濾泡性甲狀腺癌廣泛浸潤血管
四、甲狀腺癌的外科治療和常見并發癥
(一)甲狀腺癌的外科治療
1.治療原則
DTC的治療以外科治療為主,輔以術后內分泌治療、放射性核素治療,某些情況下需輔以放射治療、靶向治療。MTC以外科治療為主,某些情況下需輔以放射治療、靶向治療。未分化癌的治療,少數患者有手術機會,部分患者行放療、化療可能有一定效果,但總體來說預后很差、生存時間短。同時需要注意,腫瘤治療的個體化很重要,每一個患者病情、訴求不同,臨床診治有一定靈活性。
2.分化型甲狀腺癌的外科治療
(1)原發灶的處理
腫瘤T分級為T1、T2的病變,多局限于單側腺葉,建議行患側腺葉及峽部切除。對于部分有高危因素的患者,也可行全甲狀腺切除。這些高危因素包括:多灶癌、淋巴結轉移、遠處轉移、家族史、幼年電離輻射接觸史等。一些考慮術后有必要行核素治療的病例,也可行全甲狀腺切除。對于位于峽部的腫瘤,腫瘤較小者可行擴大峽部切除,腫瘤較大或伴有淋巴結轉移者可考慮全甲狀腺切除。
T3病變腫瘤較大或已侵犯甲狀腺被膜外肌肉,建議行全甲狀腺切除。但對于一些較靠近甲狀腺被膜的病灶,其本身可能不大,但是已經侵犯被膜外組織,可以行患側腺葉及峽部切除,同時切除受侵犯的被膜外組織。具體手術方案需權衡手術獲益和風險。
T4病變已經侵犯周圍結構器官,一般建議全甲狀腺切除。T4a病變在切除甲狀腺的同時需要切除受累的部分結構器官,如部分喉(甚至全喉)、部分氣管、下咽和部分食管等,并需要準備一定的修復方案。T4b病變一般認為屬于不可手術切除,但需根據具體情況判斷有無手術機會,可能需要血管外科、骨科、神經外科等多學科協作。但總體而言,T4b病變很難完全切凈,預后不佳,手術風險較大,術后并發癥較多。是否手術治療需要仔細評估病情,重點考慮患者能否從手術中獲益。有時,姑息性的減狀治療是必須的,例如氣管切開緩解呼吸困難等。
(2)區域淋巴結的處理
中央區淋巴結(Ⅵ區):cN1a應清掃患側中央區。如果為單側病變,中央區清掃范圍建議包括患側氣管食管溝及氣管前。喉前區也是中央區清掃的一部分,但喉前淋巴結轉移的病例不多見,可個體化處理。對于cN0的患者,如有高危因素(如T3~T4病變、多灶癌、家族史、幼年電離輻射接觸史等),可考慮行中央區清掃。對于cN0低危患者(不伴有高危因素),可個體化處理。中央區清掃的范圍,下界為無名動脈上緣水平,上界為舌骨水平,外側界為頸總動脈內側緣,包括氣管前,所以內側界為另一側的氣管邊緣。清掃該區域內的所有淋巴脂肪組織。右側需特別注意喉返神經所在水平深面的淋巴脂肪組織。需要注意保護喉返神經,同時盡可能保護甲狀旁腺及其血供,如無法原位保留甲狀旁腺則應行甲狀旁腺自體移植。
側頸部淋巴結處理(Ⅰ~Ⅴ區):DTC側頸部淋巴結轉移最多見于患側Ⅲ、Ⅳ區,其次為Ⅱ區、Ⅴ區、Ⅰ區較少見。側頸淋巴結清掃建議行治療性清掃,即術前評估或術中冰凍證實為N1b時行側頸清掃。建議側頸清掃的范圍包括Ⅱ、Ⅲ、Ⅳ、ⅤB區,最小范圍是ⅡA、Ⅲ、Ⅳ區。Ⅰ區不需要常規清掃。頸部分區示意圖和各區的具體劃分見圖1和表5。
咽旁淋巴結、上縱隔淋巴結等特殊部位淋巴結在影像學考慮有轉移時建議同期手術切除。
3.MTC的外科治療
對于MTC,建議行全甲狀腺切除。如為腺葉切除后確診的MTC,建議補充甲狀腺全切除。個別情況下,偶然發現的微小病灶MTC腺葉切除后,也可考慮密切觀察。
MTC較易出現頸部淋巴結轉移,大部分患者就診時已伴有淋巴結轉移,切除原發灶同時還需行頸部淋巴結清掃術(中央區或頸側區),清掃范圍除臨床評估外,還需參考血清降鈣素水平。MTC的手術治療宜比DTC手術略激進一些,追求徹底切除。
4.未分化癌外科治療
少數未分化癌患者就診時腫瘤較小,可能有手術機會。多數未分化癌患者就診時頸部腫物已較大,且病情進展迅速,無手術機會。腫瘤壓迫氣管引起呼吸困難時,盡可能減瘤后,行氣管切開術。
5.圍手術期治療
甲狀腺癌術后除常規補液之外,為減輕神經水腫,可給予地塞米松、神經營養類藥物輔助治療。全甲狀腺切除的患者術后注意復查甲狀旁腺素、血鈣,有低鈣癥狀者注意補充鈣劑,能進食后及時給予口服維生素D及鈣制劑。一側喉返神經損傷的患者急性期常有進食進水嗆咳,對于一些高齡患者有必要時可予鼻飼,以減少吸入性肺炎的發生。必要時在床旁置氣管切開器械包備用。雙側喉返神經損傷的患者一般術中即行氣管切開,帶氣管套管,術后注意氣管切開口的護理。頸部淋巴結清掃的患者,術后注意頸肩部的功能鍛煉。術后應根據病理分期及危險分層制訂輔助治療方案,并告知患者。
(二)常見的術后并發癥
手術并發癥是外科治療疾病過程中發生的與手術相關的其他病癥,這些病癥有一定的發生概率,并不是可以完全避免的。
1.出血
甲狀腺癌術后出血的發生率1%~2%,多見于術后24小時以內。主要表現為引流量增多,呈血性,頸部腫脹,患者自覺呼吸困難。如果引流量>100ml/h,考慮存在活動性出血,應及時行清創止血術。患者出現呼吸窘迫時應首先控制氣道,急診情況下可床旁打開切口,首先緩解血腫對氣管的壓迫。甲狀腺癌術后出血的危險因素包括合并高血壓、患者服用抗凝藥物或阿司匹林等。
2.喉返神經損傷、喉上神經損傷
甲狀腺手術喉返神經損傷的發生概率文獻報道為0.3%~15.4%。喉返神經損傷的常見原因有腫瘤粘連或侵犯神經、手術操作的原因等。如果腫瘤侵犯喉返神經,可根據情況行腫瘤削除或一并切除神經。如果切除神經,建議有條件時行一期神經移植或修復。一側喉返神經損傷,術后同側聲帶麻痹,出現聲音嘶啞、飲水嗆咳。手術操作本身可能損傷喉返神經,這種情況并不能完全避免。雙側喉返神經損傷,術后可出現呼吸困難,危及生命,手術同期應行氣管切開術,保證氣道通暢。
喉上神經損傷,患者術后聲音變低沉。術中處理甲狀腺上動靜脈時應注意緊貼甲狀腺腺體精細解剖,可減少喉上神經損傷的概率。
術中神經監測(intraoperativeneuromonitoring,IONM)技術可幫助術中定位喉返神經,可在下標本后檢測喉返神經的功能,如有神經損傷還可幫助定位損傷的節段。對二次手術、巨大甲狀腺腫物等情況、術前已有一側神經麻痹等情況,建議有條件時使用IONM。
沿被膜精細解剖、術中顯露喉返神經、合理應用能量器械、規范使用IONM可以減少神經損傷的概率。
3.甲狀旁腺功能減退
術后永久性的發生率約2%~15%,多見于全甲狀腺切除后。主要表現為術后低鈣血癥,患者出現手足發麻感、口周發麻感或手足搐搦,給予靜脈滴注鈣劑可緩解。對于暫時性甲狀旁腺功能減退,可給予鈣劑緩解癥狀,必要時加用骨化三醇。為減輕患者術后癥狀,可考慮預防性給藥。永久性甲狀旁腺功能減退者,需要終身補充鈣劑及維生素D類藥物。術中注意沿被膜的精細解剖,原位保留甲狀旁腺時注意保護其血供,無法原位保留的甲狀旁腺建議自體移植。一些染色技術可輔助術中辨別甲狀旁腺,如納米碳負顯影等。
4.感染
甲狀腺手術多為Ⅰ類切口,少部分涉及喉、氣管、食管的為Ⅱ類切口。甲狀腺術后切口感染的發生率約1%~2%。切口感染的危險因素包括癌癥、糖尿病、免疫功能低下等。切口感染的表現包括發熱、引流液渾濁、切口紅腫滲液、皮溫升高、局部疼痛伴壓痛等。懷疑切口感染,應及時給予抗菌藥物治療,有膿腫積液的,應開放切口換藥。淺表切口感染較易發現,深部切口感染常不易早期發現,可結合超聲判斷切口深部的積液。極少數患者可因感染引起頸部大血管破裂出血,危及生命。
5.淋巴漏
常見于頸部淋巴結清掃后,表現為引流量持續較多,每日可達500~1000ml,甚至更多,多呈乳白色不透明液,也稱為乳糜漏。長時間淋巴漏可致容量下降、電解質紊亂、低蛋白血癥等。出現淋巴漏后,應保持引流通暢。首先可采取保守治療,一般需禁食,給予腸外營養,數日后引流液可由乳白色逐漸變為淡黃色清亮液體,引流量也會逐漸減少。如果保守治療1~2周無明顯效果或每日乳糜液>500ml,則應考慮手術探查和結扎。手術可選擇頸部胸導管結扎、頸部轉移組織瓣封堵漏口,或者選擇胸腔鏡下結扎胸導管。
6.局部積液(血清腫)
甲狀腺術后局部積液的發生率約1%~6%。手術范圍越大其發生概率越高,主要與術后殘留死腔相關。術區留置引流管有助于減少局部積液形成。治療包括密切觀察、多次針吸積液以及負壓引流。
7.其他少見并發癥
甲狀腺手術還可引起一些其他的并發癥,但是發生率低,如氣胸(頸根部手術致胸膜破裂引起)、霍納綜合征(頸部交感神經鏈損傷)、舌下神經損傷引起伸舌偏斜、面神經下頜緣支損傷引起口角歪斜等。
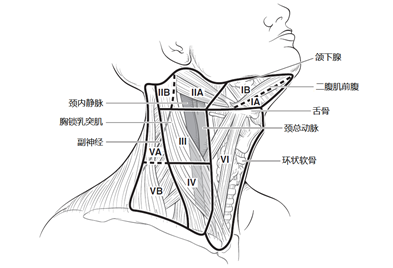
圖1頸部淋巴結分區
表5頸部淋巴結分區解剖分界
分區 | 解剖分界 | |||
上界 | 下界 | 前界(內側界) | 后界(外側界) | |
IA | 下頜骨聯合 | 舌骨 | 對側二腹肌前腹 | 同側二腹肌前腹 |
IB | 下頜骨 | 二腹肌后腹 | 二腹肌前腹 | 莖突舌骨肌 |
IIA | 顱底 | 舌骨水下緣平 | 莖突舌骨肌 | 副神經平面 |
IIB | 副神經平面 | 胸鎖乳突肌后緣 | ||
III | 舌骨下緣水平 | 環狀軟骨下緣水平 | 胸骨舌骨肌外緣 | 胸鎖乳突肌后緣 |
IV | 環狀軟骨下緣水平 | 鎖骨 | ||
VA | 胸鎖乳突肌與斜方肌交匯頂點 | 環狀軟骨下緣水平 | 胸鎖乳突肌后緣 | 斜方肌前緣 |
VB | 環狀軟骨下緣水平 | 鎖骨 | ||
VI | 舌骨 | 胸骨柄上緣 | 對側頸總動脈 | 同側頸總動脈 |
VII | 胸骨柄上緣 | 無名動脈上緣 | 頸總動脈(左) | 無名動脈 |
五、分化型甲狀腺癌的131I治療
(一)DTC術后死亡危險分層及復發危險分層
2009年ATA指南首次提出復發風險分層的概念,并于《2015ATA指南》進行了更新。該復發風險分層以術中病理特征如病灶殘留程度、腫瘤大小、病理亞型、包膜侵犯、血管侵犯程度、淋巴結轉移特征、分子病理特征及術后刺激性Tg(sTg)水平和131I治療后全身顯像(Rx-WBS)等權重因素將患者的復發風險分為低、中、高危3層。利用這一分層系統指導是否對DTC患者進行131I治療。
1.低風險分層
PTC:符合以下全部。
(1)無遠處轉移。
(2)所有肉眼所見腫瘤均被徹底切除。
(3)腫瘤未侵犯周圍組織。
(4)腫瘤不是侵襲性的組織學亞型及未侵犯血管。
(5)若行131I治療后全身顯像,未見甲狀腺床外攝碘轉移灶顯影。
(6)合并少量淋巴結轉移(如cN0,但是病理檢査發現≤5枚微小轉移淋巴結,即轉移灶最大直徑均≤0.2cm)。
(7)甲狀腺內的濾泡亞型甲狀腺乳頭狀癌;甲狀腺內的分化型甲狀腺濾泡癌合并被膜侵犯及伴或不伴輕微血管侵犯(<4處);甲狀腺內微小乳頭狀癌不論是否多灶、是否伴有BRAFV600E突變陽性,都屬于低風險分層。?
2.中風險分層
符合以下任1項。
(1)鏡下見腫瘤侵犯甲狀腺外軟組織。
(2)侵襲性組織學表現(如高細胞、靴釘樣、柱狀細胞癌等)。
(3)伴血管侵犯的甲狀腺乳頭狀癌。
(4)若行131I治療后全身顯像,可見頸部攝碘轉移灶顯影。
(5)淋巴結轉移(cN1,病理檢査發現>5枚轉移淋巴結,轉移灶最大直徑均<3cm)。?
(6)BRAFV600E突變陽性的甲狀腺腺內乳頭狀癌(直徑1~4cm)。
(7)BRAFV600E突變陽性的多灶的甲狀腺微小癌合并腺外浸潤。
3.高風險分層
符合以下任1項。
(1)明顯的腺外浸潤。
(2)癌腫未完整切除。
(3)證實存在遠處轉移。
(4)術后高Tg水平提示遠處轉移者。
(5)合并較大淋巴結轉移(任何淋巴結轉移灶直徑≥3cm)。
(6)甲狀腺濾泡癌廣泛侵犯血管(>4處血管侵犯)。?
(二)131I治療指征
1.《2015ATA指南》對高危復發危險分層患者強烈推薦131I治療。
2.對中危分層患者可考慮131I治療,但其中有鏡下甲狀腺外侵犯但癌灶較小或淋巴結轉移個數少、受累直徑小且不伴高侵襲性組織亞型或血管侵犯等危險因素的中危患者經131I治療后未能改善總體預后,可不行131I治療。
3.對低危分層患者,不推薦行131I治療。
4.《2015ATA指南》對低危人群中淋巴結受累≤5個(無節外侵犯、累及<0.2cm)者,已不再推薦行131I治療。但若從便于通過監測血清Tg水平及131I全身顯像后續隨訪的角度來看,可行131I清甲治療。
(三)131I治療禁忌證
1.妊娠期或哺乳期婦女
2.計劃6個月內妊娠者。
(四)131I清甲治療劑量
1.推薦采用30mCi進行中、低危患者的清甲治療。
2.對于伴有可疑或已證實的鏡下殘存病灶或高侵襲性組織學亞型(高細胞型、柱狀細胞型等)但無遠處轉移的中、高危患者,推薦131I輔助治療劑量為150mCi。
3.對于甲狀腺未近全切術后,需要清灶治療的患者,考慮使用較高劑量的131I。
4.頸部殘留手術未切除的DTC組織、伴發頸部淋巴結或遠處轉移,但無法手術或患者拒絕手術的、全甲狀腺切除術后不明原因血清Tg尤其是刺激性Tg水平升高者,清甲治療同時應兼顧清灶治療,131I劑量為100~200mCi。對于青少年、育齡婦女、高齡患者和腎臟功能輕中度受損的患者,可酌情減少131I劑量。
(五)TSH抑制治療的目標
1.對于高危患者,初始TSH應控制在<0.1mU/L。
2.對于中危患者,初始TSH應控制在0.1~0.5mU/L。
3.對于未檢出血清Tg的低危患者,不論是否已行131I清甲治療,TSH應控制在0.5~2mU/L。
4.對于已行131I清甲治療并且低水平Tg的低危患者,或未行131I清甲治療、Tg水平稍高的低危患者,TSH應控制在0.1~0.5mU/L。
5.對于腺葉切除患者,TSH應控制在0.5~2mU/L。
6.對于影像學療效不滿意(SIR)的患者,在沒有特殊禁忌證的情況下,TSH應無限期控制在<0.1mU/L。
7.對于血清學療效不滿意(BIR)的患者,根據初始ATA危險分層、Tg水平、Tg變化趨勢以及TSH抑制治療的不良反應,應控制TSH在0.1~0.5mU/L。
8.對于初始評為高危,但治療反應為滿意(臨床或血清學無病狀態)或療效不明確的患者,TSH控制在0.1~0.5mU/L最多5年,并隨后降低TSH抑制程度。
9.對于治療反應為滿意(臨床或血清學無病狀態)或療效不明確的患者,特別是復發危險為低危者,TSH控制在0.5~2mU/L。
10.對于未行131I清甲治療或輔助治療并且為療效滿意或療效不明確的患者,滿足頸部超聲陰性,抑制性Tg較低或未檢出,并且Tg或TgAb未呈增高趨勢,TSH控制在0.5~2mU/L。
(六)局部或遠處轉移患者的應用131I清灶治療的原則
1.對于無法手術切除的攝碘病灶推薦131I治療。最大耐受劑量上限為150mCi。
2.對于肺轉移的治療,病灶仍攝取碘并出現臨床有效,每隔6~12個月再次施行治療。經驗性治療劑量推薦為100~200mCi,對于70歲以上患者的劑量為100~150mCi。
3.對于骨轉移灶,劑量為100~200mCi。
4.中樞神經系統轉移都應當首先考慮外科手術或立體定向外照射。
(七)Tg陽性131I全身掃描陰性患者的治療原則
1.對于停服L-T4所致的sTg<10ng/ml或應用rhTSH所致的sTg<5ng/ml的患者,續行TSH抑制治療,并密切隨訪,但若血清Tg逐漸升高或存在疾病進展(PD)的其他證據,可行131I經驗性治療。
2.對于停服L-T4所致的sTg>10ng/ml或應用rhTSH所致的sTg>5ng/ml,Tg或TgAb水平持續升高,并且頸部、胸部影像學、18F-FDGPET-CT陰性的患者,可行131I經驗性治療,劑量100~200mCi。但若Rx-WBS仍為陰性,則將其歸為碘難治性DTC的范疇,需終止131I治療。
六、甲狀腺癌的放射治療
甲狀腺癌對放射治療敏感性差,單純放射治療對甲狀腺癌的治療并無好處,外照射放療僅在很小一部分患者中使用。放射治療原則上應配合手術使用,主要為術后放射治療。
具體實施應根據手術切除情況、病理類型、病變范圍、年齡等因素而定。
1.對惡性程度較低的癌如分化好的乳頭狀癌或濾泡癌僅在無法再次手術切除時才考慮介入。
2.當腫瘤累及較重要的部位如氣管壁、氣管食管溝、喉、動脈壁或靜脈內有瘤栓等而手術又無法切除干凈,且131I治療又因殘存較大無明顯效果時才可考慮術后放射治療。
3.對年輕患者,病理類型一般分化較好,即使出現復發轉移也可帶瘤長期存活,且131I治療和再次手術都為有效的治療手段,應慎用外照射。
4.對分化差的癌或未分化癌,如手術后有殘留或廣泛淋巴結轉移,應及時給予大范圍的術后放射治療,以盡可能地降低局部復發率,改善預后。
(一)放射治療指征
1.高分化的乳頭狀腺癌和濾泡狀腺癌
目前國際上廣泛采取的外照射的指征見圖2。
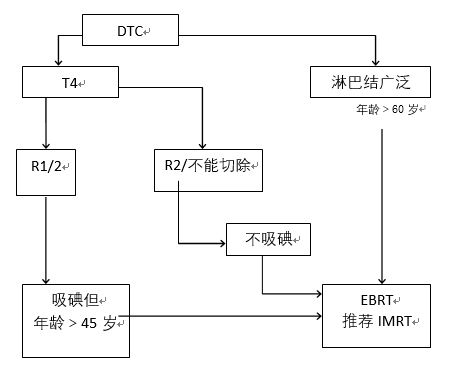
圖2.DTC的放療指征
中國醫學科學院腫瘤醫院放療科外照射的指征包括:①腫瘤肉眼殘存明顯而且不能手術切除,單純依靠放射性核素治療不能控制者;②術后殘存或復發病灶不吸碘者。
2.髓樣癌
外照射治療:對手術不能全切,或是復發的患者,是否應該進行外照射尚缺乏有力的證據,但是通常認為外照射有助于這些患者的局部控制。
髓樣癌的外照射指征見圖3。
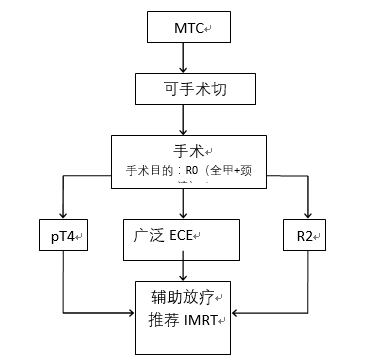
圖3髓樣癌的放療指征
3.未分化癌(ATC)
綜合治療是主要的治療方式,而且要根據患者的具體情況,進行個體化的治療。
外照射治療:放療可作為術前、術后綜合治療的一部分發揮作用。也可以采用單純放療,可行高劑量放療(推薦劑量高達60Gy)
4.甲狀腺癌遠處轉移病灶姑息放療
甲狀腺癌出現遠處轉移病灶如肺、肝、骨、腦且伴有臨床癥狀,可以考慮手術/RAI聯合EBRT/SBRT,以減輕癥狀,減緩腫瘤進展。
(二)外照射技術
1.放療前應詳細檢查以明確腫瘤的具體清況,為靶區的制定作準備
(1)對出現聲嘶、吞咽困難、喘鳴者表明腫瘤已侵出甲狀腺體范圍而達喉返神經、食管、氣管等。
(2)頸部詳細檢查有無腫大淋巴結以確定有無區域性淋巴結轉移。
(3)間接喉鏡檢查以明確有無聲帶麻痹而肯定是否有喉返神經受侵。
(4)頸部超聲、CT可用于明確腫瘤具體侵犯范圍及頸部淋巴結腫大情況;X線胸片,腹部超聲、骨掃描應常規檢查以除外遠地轉移的可能。
(5)術后放療者應詳細了解手術情況、術后有無殘留及術后病理結果。
2.照射劑量
甲狀腺外照射劑量通常分為大分割方案和常規分割放療方案。按常規劑量分割方式:分次劑量200cGy,每日1次,每周5次,大野照射5000cGy,然后縮野針對殘留區加量至6000~7000cGy,注意脊髓量勿超過耐受量。美國頭頸學會(AmericanHeadandNeckSociety,AHNS)的治療劑量指南:對于有肉眼殘留的病灶,通常給予70Gy,對于鏡下殘留或者腫瘤經手術剔除的區域66Gy,高危微小病灶殘留區域(包括甲狀腺床、氣管食管溝、Ⅵ區淋巴結引流區)60Gy,低危為小病灶區域(包括未受侵的Ⅲ~Ⅴ區、上縱隔淋巴結)54~56Gy。
部分研究顯示對于分化型甲狀腺癌,可采用大分割方式,單次劑量2.5~3.0Gy,可以獲得更好的局部控制。這個結論尚需進一步的研究證實。
3.外照射的并發癥
急性并發癥:1~2度的反應較常見,約在80%以上,包括咽炎、黏膜炎、口干、味覺改變、吞咽困難、吞咽疼痛、放射性皮炎等。3度以上的反應少見,咽炎的發生率最高(<10%),其余反應<5%。
晚期并發癥:包括皮膚肌肉纖維化,食管氣管狹窄,咽部狹窄導致吞咽困難,頸內動脈硬化,第二原發癌等。
七、甲狀腺癌的全身治療
內科治療對部分對放射性碘治療不敏感并出現遠處轉移患者和甲狀腺未分化癌有效。化療對分化型甲狀腺癌療效差,靶向治療更為重要;而對甲狀腺未分化癌主要的內科治療是化療。
(一)分子靶向治療
1.分化型甲狀腺癌存在血管內皮生長因子(VEGF)及其受體(VEGFR)的高表達和諸如RET異位、BRAFV600E突變、RAS點突變等變異。作用于這些靶點的多激酶抑制劑可延長中位無進展生存期,并使部分患者的腫瘤縮小。
2.對于進展較迅速,有癥狀的晚期放射性碘難治性分化型甲狀腺癌(乳頭狀癌、濾泡狀癌和Hürthle細胞癌)患者,可考慮使用多激酶抑制劑索拉非尼。索拉非尼在我國獲批的適應證是:局部復發或轉移的進展性的放射性碘難治性(RAI)分化型甲狀腺癌。
3.對于進展較迅速,有癥狀的晚期甲狀腺髓樣癌患者,國外指南推薦vandetanib和cabozantinib。
(二)化學治療
對于ⅣA期和ⅣB期甲狀腺未分化癌,可考慮在放療基礎上加用化療。化療可以與放療同步使用,也可在放療后輔助性給予。使用的藥物包括紫杉類、蒽環類和鉑類,具體方案見表6。同步化放療時,化療方案推薦采用每周方案。
對于ⅣC期甲狀腺未分化癌,可考慮給予全身化療。推薦用于ⅣC期甲狀腺未分化癌的方案包括紫杉醇聯合鉑類、多西紫杉醇聯合多柔比星、紫杉醇單藥、多柔比星單藥。具體方案見表7。
表6用于ⅣA期和ⅣB期甲狀腺癌未分化癌輔助化療或同步化放療的化療方案
方案 | 藥物/劑量 | 頻度 |
紫杉醇/卡鉑 | 紫杉醇 50 mg/m2,卡鉑 AUC 2 mg/m2 靜脈注射 | 每周 |
多西他賽/多柔比星 | 多西他賽 60 mg/m2 靜脈注射,多柔比星 60 mg/m2 靜脈注射(須聚乙二醇化非格司亭支持) | 每3~4 周 |
多西他賽/多柔比星 | 多西他賽 20 mg/m2 靜脈注射,多柔比星 20 mg/m2 靜脈注射 | 每周 |
紫杉醇 | 30~60 mg/m2 靜脈注射 | 每周 |
順鉑 | 25 mg/m2 靜脈注射 | 每周 |
多柔比星 | 60mg/m2 靜脈注射 | 每3周 |
多柔比星 | 20 mg/m2 靜脈注射 | 每周 |
表7. 用于IVC期甲狀腺未分化癌的化療方案
方案 | 藥物/劑量 | 頻度 |
紫杉醇/卡鉑 | 紫杉醇 60~100 mg/m2,卡鉑 AUC 2 mg/m2 靜脈注射 | 每周 |
紫杉醇/卡鉑 | 紫杉醇 135~175 mg/m2,卡鉑 AUC 5~6 mg/m2 靜脈注射 | 每3~4 周 |
多西他賽/多柔比星 | 多西他賽 60 mg/m2 靜脈注射,多柔比星 60 mg/m2 靜脈注射(聚乙二醇化非格司亭支持) | 每3~4 周 |
多西他賽/多柔比星 | 多西他賽 20 mg/m2 靜脈注射,多柔比星 20 mg/m2 靜脈注射 | 每周 |
紫杉醇 | 60~90 mg/m2 靜脈注射 | 每周 |
紫杉醇 | 135~200 mg/m2 靜脈注射 | 每3~4 周 |
多柔比星 | 60~75 mg/m2 靜脈注射 | 每3周 |
多柔比星 | 20 mg/m2 靜脈注射 | 每周 |
八、甲狀腺癌的中醫中藥治療
甲狀腺癌在中醫學中屬癭瘤范疇,現代研究結合古代醫家對本病的認識,都認為情志因素是本病發病的主要原因,此外還與虛、痰、瘀、熱、毒、飲食關系密切,臨床常見虛實兼雜,多因素相雜共同致病。
(一)辨證論治
目前,中醫在治療甲狀腺癌方面一是配合手術、化療、放療,減輕化療、放療以及術后的負荷,在減輕不良反應、提高體力、改善食欲、抑制腫瘤發展、控制病情等方面起到輔助治療及終末期支持治療作用;二是作為不接受手術和放化療患者的主要治療手段。
適應人群:圍手術期、放化療、靶向治療期間、治療后恢復期及晚期患者。
治療方法:口服湯藥,中藥制劑,中成藥,其他中醫療法(外敷、針灸等)。
(二)治療方案
1.正氣虧虛
常見于先天身體虛弱或手術、放化療后損傷正氣。
代表方劑:八珍湯、當歸補血湯、十全大補湯、補中益氣湯加減。
2.陰虛火旺
常見于放療后或素體不足。
代表方劑:知柏地黃丸加減。
3.肝腎不足
常見于放化療后骨髓抑制或素體不足。
代表方劑:六味地黃丸加減。
4.肝郁氣滯
代表方劑:海藻玉壺湯或半夏厚樸湯加減。
5.寒痰凝滯
代表方劑:陽和湯合半夏消瘰丸加減。
6.毒瘀互結
代表方劑:西黃丸或小金丹加減。
九、甲狀腺癌多學科綜合治療模式和隨訪
(一)甲狀腺癌的多學科綜合治療模式
甲狀腺癌尤其是分化型甲狀腺癌(DTC)預后良好,死亡率較低,有較長的生存期。一般需要多學科規范化的綜合診治過程,包括外科、病理科、影像診斷科、核醫學科、放療科、內分泌科、腫瘤內科等,針對不同的患者或者同一患者的不同治療階段應實施個體化精準治療。
甲狀腺癌的治療、隨訪過程中應以外科為主導。根據患者不同病情與核醫學科、內分泌科、放療科、腫瘤內科等共同協商制訂個體化的綜合治療方案。
1.對于低危分化型甲狀腺癌患者,外科手術+術后的外源性甲狀腺素的替代治療或TSH抑制治療即可。
2.對于遠處轉移高危分化型甲狀腺癌患者,外科手術+術后131I治療+術后TSH抑制治療是主要的綜合治療模式。
3.對于不可手術切除的局部病灶,可以考慮局部射頻消融或外照射。
4.甲狀腺髓樣癌的治療應以外科治療為主,不需要TSH抑制治療,但需要甲狀腺素補充治療。
5.對于甲狀腺未分化癌,如果無遠處轉移和氣道梗阻,可首選外照射+手術/手術+外照射。外科的作用主要是解除氣道梗阻(氣管切開),在條件許可的情況盡量切除腫瘤。
(二)甲狀腺癌的術后隨訪
對甲狀腺癌患者進行長期隨訪的目的在于:①對臨床治愈者進行監控,以便早期發現復發腫瘤和轉移;②對DTC復發或帶瘤生存者,動態觀察病情的進展和治療效果,調整治療方案;③監控TSH抑制治療的效果;④對DTC患者的某些伴發疾病(如心臟疾病、其他惡性腫瘤等)病情進行動態觀察。
1.分化型甲狀腺癌(DTC)術后需要給予外源性甲狀腺素抑制治療。根據術后復發危險度決定TSH抑制治療的程度。每次調整口服外源性甲狀腺素的劑量后,4~6周隨訪復查甲狀腺功能,待達到理想的平衡點后可酌情延長隨訪間隔,3~6個月復查1次,如有不適可隨時檢測甲狀腺功能。
2.對已清除全部甲狀腺(手術和131I清甲后)的DTC患者,應定期檢測血清Tg水平,建議采用同種檢測試劑。對血清Tg的長期隨訪從131I清甲治療后6個月起開始,此時檢測基礎Tg(TSH抑制狀態下)或TSH刺激后(TSH>30mU/L)的Tg。131I治療后12個月,復查測定TSH刺激后的Tg。隨后,每6~12個月復查基礎Tg。復發危險度中、高危者可在清甲治療后3年內復查TSH刺激后的Tg。
3.DTC隨訪期間應定期進行頸部超聲檢查,評估甲狀腺床和頸部中央區、側頸部的淋巴結狀態。術后首次超聲檢查建議為:高危患者術后3個月,中、低危患者術后6個月。如發現可疑病灶,檢查間隔可酌情縮短。對可疑淋巴結可行超聲引導下穿刺活檢和/或穿刺針沖洗液的Tg檢測。
4.DTC患者在手術和131I清甲治療后,可根據復發危險度,在隨訪中選擇性應用Dx-WBS。
(1)中低危復發風險度的DTC患者如Dx-WBS未提示甲狀腺床以外的131I攝取,并且隨訪中頸部超聲無異常、基礎血清Tg水平(TSH抑制狀態下)不高,無需進行Dx-WBS。
(2)中高危復發危險度的DTC患者,長期隨訪中應用Dx-WBS對發現腫瘤病灶可能有價值,建議檢查間隔6~12個月。如果患者在隨訪中發現Tg水平逐漸升高,或者疑有DTC復發,可行Dx-WBS檢查。
5.CT和MRI不是DTC隨訪中的常規檢查項目。在下述情況時應行頸胸部CT或MRI檢查:①淋巴結復發廣泛,彩超無法準確描述范圍;②轉移病灶可能侵及上呼吸消化道,需要進一步評估受侵范圍;③高危患者中血清Tg水平增高(>10ng/ml)或者TgAb升高。而Dx-WBS陰性時如可能進行后續131I治療,檢查時應避免使用含碘對比劑。若行含碘對比劑的增強掃描,建議在掃描后4~8周行131I治療。
6.目前不推薦在DTC隨訪中常規使用18F-FDGPET顯像,但在下述情況下可考慮使用
(1)血清Tg水平增高(>10ng/ml)而Dx-WBS陰性時,協助尋找和定位病灶。
(2)對病灶不攝碘者,評估和監測病情。
(3)對侵襲性或轉移性DTC者,評估和監測病情。
7.DTC的長期隨訪還應納入以下內容
(1)131I治療的長期安全性:包括對繼發性腫瘤、生殖系統的影響。但應避免過度篩查和檢查。
(2)TSH抑制治療的效果:包括TSH抑制治療是否達標、治療的不良反應等。
(3)DTC患者的伴發疾病:由于某些伴發疾病(如心臟疾病、其他惡性腫瘤等)的臨床緊要性可能高于DTC本身,所以長期隨訪中也要對上述伴發疾病的病情進行動態觀察。
(三)發現DTC復發或轉移后的處理
局部區域復發或轉移可發生于甲狀腺殘留組織、頸部軟組織和淋巴結,遠處轉移可發生于肺、骨、腦和骨髓等。針對復發或轉移病灶,可選擇的治療方案依次為:手術切除(可能通過手術治愈者首選手術治療)、131I治療(病灶可以攝碘者)、外照射治療、TSH抑制治療情況下觀察(腫瘤無進展或進展較慢,并且無癥狀、無重要區域如中樞神經系統等受累者)、化學治療和新型靶向藥物治療及獲批的藥物臨床試驗(疾病迅速進展的難治性DTC患者)。最終采取的治療方案必須考慮患者的一般狀態、合并疾病和既往對治療的反應。甲狀腺已完全清除的DTC患者,在隨訪中血清Tg水平持續增高(>10ng/ml),但影像學檢查未發現病灶。對這類患者,可經驗性給予3.7~7.4GBq(100~200mCi)131I治療;如治療后Dx-WBS發現DTC病灶或血清Tg水平減低,可重復131I治療,否則應停止131I治療,以TSH抑制治療為主。
(四)甲狀腺髓樣癌術后隨訪
術后甲狀腺功能的隨訪與DTC一致,但不需要TSH抑制治療。由于血清降鈣素和CEA與甲狀腺髓樣癌有較好的特異性,為隨訪復查時的必查項目。對于手術后血清降鈣素和CEA水平恢復正常的患者,其隨訪期可參考低危分化型甲狀腺癌;對于血清降鈣素和CEA盡管沒有恢復正常,但處于較低水平者,可參考高危分化型甲狀腺癌患者;對于仍處于較高水平的患者,應密切隨訪,建議3~6個月復查超聲,并根據血清降鈣素和CEA上升的幅度,結合CT或MRI明確腫瘤范圍,必要時行PET-CT檢查。
附件1
第7版AJCC甲狀腺癌分期
美國癌癥聯合會(AJCC)甲狀腺癌 TNM 分類(第7版2010) | |
原發灶(T) 注:所有分類都可以分為:(s)單灶和(m)多灶(最大者直徑決定分期) | |
Tx | 原發腫瘤不能評價 |
T0 | 沒有原發腫瘤證據 |
T1 | T1腫瘤最大直徑≤2cm 且局限在甲狀腺內 |
T1a | 腫瘤最大直徑<1cm且局限在甲狀腺內 |
T1b | 腫瘤最大直徑大于1cm且≤2cm且局限在甲狀腺內 |
T2 | 腫瘤最大直徑大于2cm且≤4cm且局限在甲狀腺內 |
T3 | 腫瘤最大直徑>4cm 且局限在甲狀腺內或有任何微小腺體外侵犯(如侵犯帶狀肌或甲狀腺周圍脂肪組織) |
T4a | 任何大小腫瘤侵犯甲狀腺包膜以外至皮下軟組織、喉、氣管、食管或喉返神經 |
T4b | 腫瘤侵犯椎前筋膜或包裹頸動脈或縱隔血管 |
所有未分化癌歸為T4期 | |
T4a | 腺體內未分化癌 |
T4b | 肉眼侵犯腺體外的未分化癌 |
區域淋巴結(N) (包括中央區淋巴、頸側區淋巴結和上縱隔淋巴結) | |
Nx | 區域淋巴結不能評估 |
N0 | 無區域淋巴結轉移 |
N1 | 區域淋巴結轉移 |
N1a | 腫瘤轉移至Ⅵ區(氣管前、氣管旁、喉前/Delphian淋巴結) |
N1b | 腫瘤轉移至單側、雙側或對側頸部(Ⅰ、Ⅱ、Ⅲ、Ⅳ或Ⅴ區),或咽后淋巴結,或上縱隔淋巴結(Ⅶ區) |
遠處轉移(M) | |
M0 | 無遠處轉移灶 |
M1 | 有遠處轉移灶 |
美國癌癥聯合會(AJCC)甲狀腺癌TNM分期(第7版2010)
美國癌癥聯合會(AJCC)甲狀腺癌 TNM 分期(第7版2010) | |||||||
乳頭狀或濾泡狀癌(分化型) | 髓樣癌(所有年齡組) | ||||||
年齡<45歲 | T | N | M | ||||
T | N | M | Ⅰ期 | 1 | 0 | 0 | |
Ⅰ期 | 任何 | 任何 | 0 | Ⅱ期 | 2 | 0 | 0 |
Ⅱ期 | 任何 | 任何 | 1 | 3 | 0 | 0 | |
年齡≥45歲 | Ⅲ期 | 1 | 1a | 0 | |||
Ⅰ期 | 1 | 0 | 0 | 2 | 1a | 0 | |
Ⅱ期 | 2 | 0 | 0 | 3 | 1a | 0 | |
Ⅲ期 | 3 | 0 | 0 | ⅣA | 4a | 0 | 0 |
1 | 1a | 0 | 4a | 1a | 0 | ||
2 | 1a | 0 | 1 | 1b | 0 | ||
3 | 1a | 0 | 2 | 1b | 0 | ||
ⅣA期 | 4a | 0 | 0 | 3 | 1b | 0 | |
4a | 1a | 0 | 4a | 1b | 0 | ||
1 | 1b | 0 | ⅣB期 | 4b | 任何 | 0 | |
2 | 1b | 0 | ⅣC期 | 任何 | 任何 | 1 | |
3 | 1b | 0 | 所有未分化癌歸為Ⅳ期 | ||||
4a | 1b | 0 | ⅣA期 | 4a | 任何 | 0 | |
ⅣB期 | 4b | 任何 | 0 | ⅣB期 | 4b | 任何 | 0 |
ⅣC期 | 任何 | 任何 | 1 | ⅣC期 | 任何 | 任何 | 1 |
(責任編輯:)