群雄逐鹿PD-1/PD-L1抗體專利
PD-1/PD-L1抗體是當前腫瘤免疫治療領域最受關注的熱點之一,在我國已有4個藥物獲批上市,分別是百時美施貴寶的納武利尤單抗注射液(Opdivo)、默沙東的帕博利珠單抗注射液(Keytruda)、君實生物的特瑞普利單抗注射液、信達生物的信迪利單抗注射液,此外,多款國產生物類似藥已提交上市申請。而如何進行PD-1/PD-L1抗體的專利布局,也是近年來國內外藥企關注的重點。
我國專利申請趨勢
2017年1月,百時美施貴寶與默沙東就PD-1抗體全球專利戰達成和解,作為和解協議的一部分,默沙東首期將向百時美施貴寶方支付6.25億美元的費用,并將基于默沙東的Keytruda從2017年至2026年的全球(包括美國、英國、荷蘭、法國、德國、愛爾蘭、西班牙、瑞士、澳大利亞和日本)銷售額,持續支付6.5%(2017年1月1日~2023年12月31日)或2.5%(2024年1月1日~2026年12月31日)的專利許可費。自此,百時美施貴寶與默沙東的PD-1抗體專利大戰落下帷幕。
百時美施貴寶與默沙東進行的PD-1抗體專利大戰,由于各個國家對PD-1抗體專利的授權標準、范圍不同,基本沒有波及我國市場。在國際市場激烈競爭的情況下,我國PD-1抗體藥物迅猛發展,而國內各企業的相關專利申請布局情況則相對比較平靜。
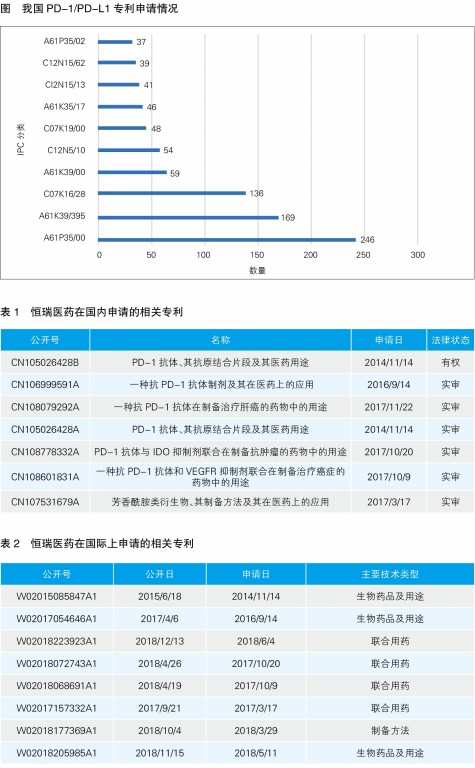
在我國,2014年以前以PD-1/PD-L1為靶點的藥物的相關專利申請較少,趨勢平緩;2014年,申請量開始增加,趨勢陡升;2016年左右,申請量最多,接近160件,達到頂峰;近兩年申請量有所下降。由申請的技術類型可以看出,國內PD-1/PD-L1抗體專利的授權范圍多為國際專利分類(IPC)中的A61P35/00 抗腫瘤藥,其次為A61K39/395抗體、免疫球蛋白、免疫血清等(見圖)。具體保護范圍包括抗體的序列片段、組合物、用途、方法、醫療器械等具體而狹小的某一方面的產品或用途,而涉及功能性保護較廣的授權范圍在我國很難拿到專利授權保護。例如,在百時美施貴寶與默沙東PD-1抗體專利大戰中的關鍵性專利Opdivo的基礎專利WO2004004771A1,該專利權利要求利用功能性限定“通過抑制PD-1,PD-L1或PD-L2等免疫抑制信號通路而使免疫增強的方法治療癌癥或者感染”保護了相當大的范圍,這在我國是很難獲得授權的。
國內企業紛紛“出手”
近年來,國內企業積極布局PD-1/PD-L1抗體有關專利。
恒瑞醫藥具有較強的知識產權保護意識,不僅在國內布局抗體產品、用途、制劑、組合物及聯合用藥等多方面專利,也非常重視海外市場的專利布局,相繼到美國、澳大利亞、巴西等國家和地區申請相關專利(恒瑞醫藥在國內外申請的專利情況見表1、表2)。
百濟神州在我國申請的5件專利中,目前已有1件獲得授權。該專利權利要求為 “一種抗體或其片段,所述抗體或其片段特異性結合人類PD-1且包含以下6個互補決定區(CDR),其中CDR-H1的序列如序列編號31所示、CDR-H2的序列如序列編號32所示、CDR-H3的序列如序列編號33所示、CDR-L1的序列如序列編號34所示、CDR-L2的序列如序列編號35所示和CDR-L3的序列如序列編號36所示。”該專利保護范圍較具體,且沒有布局任何周邊相關專利,專利保護力度較弱。百濟神州從2015年開始在海外進行專利布局,分別在美國、韓國、印度等國家和地區,就生物藥產品、組合物、聯合用藥、適應證、制備方法等申請專利保護。如果想在激烈的PD-1抗體市場競爭中獲得優勢,企業需在國內外同時擴大專利保護網絡,加強知識產權保護力度,且在面對激烈的海外競爭時做好專利防御及主動進攻的專利策略。
信達生物在國內布局了PD-1單抗產品、用途、組合物、適應證等一系列周邊專利,目前這些專利均在實審狀態,尚無授權專利,知識產權保護力度較為薄弱。國際專利布局方面,已在歐洲、澳大利亞、加拿大等國家和地區提出專利申請,申請日期多在2016年以后,目前尚未有授權專利。建議加強研究,盡早申請專利,并利用一切方法延長專利保護期,以防競爭對手搶占先機。
君實生物于2013年獲得蘇州君盟生物醫藥科技有限公司的專利CN104250302B,其權利要求保護了:“1. 能夠結合PD-1的抗體或其功能性片段,其重鏈CDR1、CDR2和CDR3以及輕鏈CDR1、CDR2和CDR3的氨基酸序列選自以下各氨基酸序列的組中的一組。2. 權利要求1所述的抗體或其功能性片段,其包含選自氨基酸序列SEQ ID NO:19,21, 23的重鏈可變區,和選自氨基酸序列SEQ ID NO:20,22,24的輕鏈可變區。”該專利保護了幾組具體的氨基酸序列、片段、載體、制備方法及適應證乳腺癌或黑色素瘤。
君實生物另一篇專利CN108456251A權利要求為:“1. 抗體或其功能性片段,其包含選自氨基酸序列SEQ ID NO:7,8,9,13,14,15,19,20,21 ,22,23,24,28,29,30或任何所述序列之變體的重鏈CDR,和/或選自氨基酸序列SEQ ID
NO:1,2,3,4,5,6,10,11,12,16,17,18,25,26,27或任何所述序列之變體的輕鏈CDR。2. 權利要求1所述的抗體或其功能性片段,其中所述重鏈CDR的CDR1、CDR2和CDR3的氨基酸序列選自以下各氨基酸序列或其變體的組中的一組:
HCDR1 HCDR2 HCDR3A SEQ ID NO:7 SEQ ID NO:8 SEQ ID NO:9B SEQ ID NO:13 SEQ ID NO:14 SEQ ID NO:15C SEQ ID NO:19 SEQ ID NO:20 SEQ ID NO:21D SEQ ID NO:22 SEQ ID NO:23 SEQ ID NO:24E SEQ ID NO:28 SEQ ID NO:29 SEQ ID NO:30和/或所述輕鏈CDR的CDR1、CDR2和CDR3的氨基酸序列選自以下各氨基酸序列或其變體的組中的一組。”
對比以上兩專利可以看出,君實生物在2017年申請的PD-L1抗體專利擴大了序列范圍,擴展了結合PCSK9的抗體聯合用藥的新用途。盡管如此,相較注重知識產權保護的跨國公司,君實生物在PD-L1抗體藥物的專利保護方面在國內較為薄弱(僅有三篇相關專利),海外市場分別進入美國、巴西、印度,海外專利保護力度較為薄弱,專利保護力度仍需加強。
專利布局越早越好
從國內藥企申請的PD-1抗體有關專利信息可以看出,相較于跨國企業全面且堅實的專利壁壘,國內企業對于知識產權的布局尚處于起步階段,唯有恒瑞醫藥有重視海外市場專利布局的意識。國外企業在PD-1靶點研發與專利布局的策略,值得國內企業參考學習。
一方面,國內企業在生物藥方面投入的人力、物力、財力逐漸加大,在研發前期即應將專利布局提上日程,盡早保護核心專利,同時申請周邊專利,編織一個合理、有效的專利保護網,從而使自身的利益最大化。
另一方面,更要重視后續的研發。企業可以對已經公開的專利技術進行相應改進,如抗體功能區氨基酸的突變、結構的改變、提高生物活性等一系列產品技術的改進;對相應劑型、組合物、適應證、制備方法可以進行更多的嘗試。同時,要對改進的新技術及時申請專利進行全面保護,構建自己的專利網,必要時通過專利訴訟、專利復審等法律手段達到和解機會或交互許可的目的,實現與競爭對手相互制衡,以便在未來的市場競爭中占據一席之地。(趙晶 趙琨)