近期美國Clinicaltrial數據庫臨床試驗數據顯示—— 我國三家藥企研發活躍度躋身全球前十
- 2026-01-29 11:02
- 作者:陳宇哲
- 來源:中國醫藥報
根據美國Clinicaltrial數據庫數據,2025年12月份,全球新開由企業資本主導的臨床試驗總數為868項,數量環比上升43.47%;單月新開臨床試驗數量高于2024年同期水平,同比上漲28.59%。值得注意的是,我國有3家企業進入新開臨床試驗數量排名前十榜單,分別為圣釋生物、百利天恒和金賽藥業。
熱門領域分布
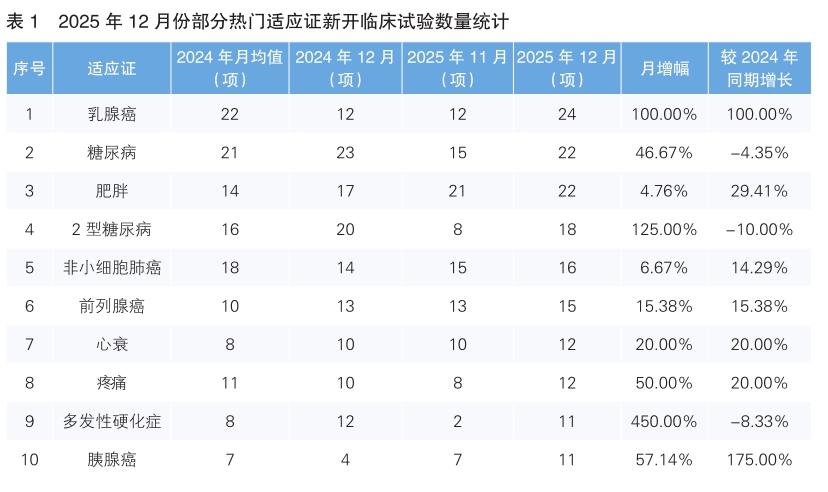
從2025年12月份新開臨床試驗適應證來看,乳腺癌為最熱門的研發領域,新開臨床試驗24項,環比同比均翻一番。值得一提的是,2025年12月份針對熱門適應證新開臨床試驗數量環比均呈上升趨勢,其中多發性硬化癥上升幅度最大,新開臨床試驗11項,環比增長450%。(詳見表1)
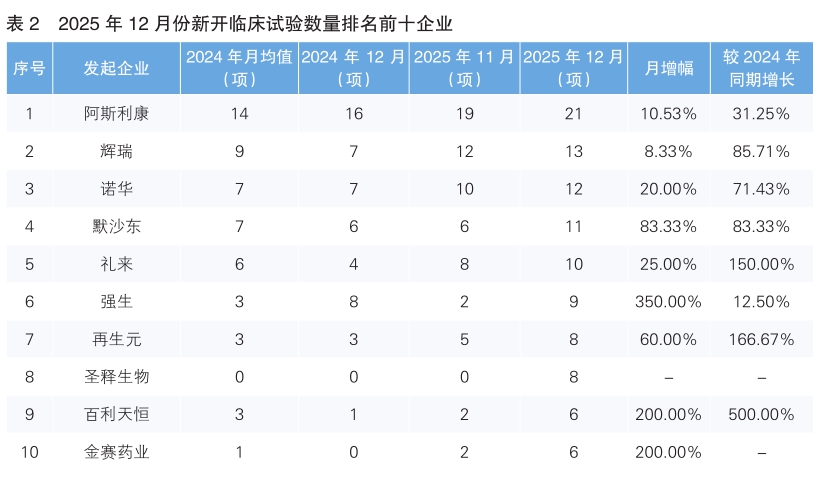
對新開臨床試驗的發起單位進行統計后發現,2025年12月份發起臨床試驗最多的企業是阿斯利康,新開臨床試驗21項,環比上升了10.53%,同比增長了31.25%。其次為輝瑞,新開臨床試驗13項,環比上升了8.33%,同比增長了85.71%。新開臨床試驗數量上升幅度最大的企業為強生,環比上升350%。值得注意的是,2025年12月份我國藥企圣釋生物、百利天恒和金賽藥業進入新開臨床試驗數量排名前十榜單,分別新開臨床試驗8項、6項、6項。(詳見表2)
對臨床試驗的申請國家和地區進行統計后發現,2025年12月份美國仍為臨床試驗開展最為主要的國家,新開臨床試驗266項;其次是中國,新開臨床試驗數量為151項。2025年12月份新開臨床試驗數量月降幅最大的是韓國,環比下降35.29%。
頭部企業表現
阿斯利康2025年12月份新開的21項臨床試驗中,僅有1項Ⅲ期臨床試驗,試驗藥物為Rilvegostomig,適應證為膽管癌(NCT07221253)。Rilvegostomig是阿斯利康基于DuetMab分子骨架構建的一款PD-1/ TIGIT雙特異性單克隆抗體,采用單價人源化IgG1抗體結構,并對Fc區域進行三重突變,以最大程度弱化Fc介導的免疫效應功能。其核心作用機制在于同時阻斷PD-1和TIGIT兩個免疫檢查點蛋白,進而解除腫瘤微環境對T細胞的抑制效應,增強抗腫瘤免疫反應。
輝瑞2025年12月份新開的13項臨床試驗中,有4項為Ⅲ期臨床試驗,涵蓋3款生物藥與1款化學藥。化學藥的Ⅲ期臨床試驗藥物為Abrocitinib,適應證為特應性皮炎(NCT06807281)。Abrocitinib是全球首款高選擇性口服Janus激酶1(JAK1)抑制劑,能夠高選擇性阻斷JAK1激酶活性,對JAK2/ JAK3/TYK2的抑制活性極低,有效規避了非選擇性JAK抑制劑引發的廣譜副作用。3項生物藥Ⅲ期臨床試驗中有2項試驗藥物均為PF-08634404(原研代號:SSGJ-707),適應證分別為小腸腫瘤(NCT07222800)與晚期非小細胞肺癌(NCT07222566)。該藥由輝瑞自我國藥企三生制藥引進,為PD-1/VEGF雙特異性抗體,可同時作用于PD-1免疫檢查點與VEGF血管生成因子,實現“免疫激活+抗血管生成”的雙重抗腫瘤作用。另1項Ⅲ期臨床試驗的生物藥為C.difficile疫苗,適應證為艱難梭菌相關疾病(NCT07282665)。
默沙東2025年12月份新開的11項臨床試驗中,僅1項推進至Ⅲ期臨床,適應證為子宮頸癌(NCT07216703),試驗藥物為Pembrolizumab與Tirumotecan的聯合療法。該聯合方案采用PD-1抑制劑+TROP2靶向抗體偶聯藥物(ADC)的協同治療策略,通過免疫激活與靶向化療雙重機制殺傷腫瘤細胞;目前正處于多項Ⅲ期臨床試驗階段,主要針對非小細胞肺癌、三陰性乳腺癌、子宮內膜癌等實體瘤,旨在提升一線治療及維持治療效果,克服單藥治療耐藥性問題。
禮來2025年12月份新開的10項臨床試驗中,有3項為Ⅲ期臨床試驗,其中1項Ⅲ期臨床試驗的試驗藥物為Eloralintide,適應證為超重(NCT07282600)。Eloralintide是一款每周一次皮下注射的高選擇性胰淀素受體激動劑,適用于肥胖癥及2型糖尿病的治療。其作用機制為模擬內源性胰淀素的生理功能,調節飽腹感、延緩胃排空并抑制胰高血糖素分泌,從而實現顯著減重效果。該藥可優先激活胰淀素受體(AMY1R、AMY2R、AMY3R),對降鈣素受體的選擇性較低。另外2項Ⅲ期臨床試驗均為腫瘤治療研究,其中1項試驗藥物為LY4064809,適應證為乳腺癌(NCT07174336)。LY4064809是一款高選擇性、變構型PI3Kα抑制劑,專門針對攜帶PIK3CA基因突變的HR+/HER2-晚期乳腺癌,通過精準靶向腫瘤細胞中的突變型 PI3Kα,在增強治療效果的同時,減少對正常細胞的影響,降低代謝相關不良反應發生率。另1項Ⅲ期臨床試驗的試驗藥物為Vepugratinib,適應證為移行細胞癌(NCT07218380)。該藥是一款口服、高效、亞型選擇性小分子FGFR3抑制劑,其核心優勢在于對FGFR3的高度特異性,對FGFR1/2/4的抑制活性極低,可顯著降低脫靶毒性。
金賽藥業2025年12月份新開的6項臨床試驗中,包括1項Ⅱ期臨床、1項Ⅰ/Ⅱ期臨床和4項Ⅰ期臨床。其中,Ⅱ期與Ⅰ/Ⅱ期臨床的試驗藥物均為GS3-007a,適應證分別為成人生長激素缺乏癥(NCT07259564)和兒童生長激素缺乏癥(NCT07264595)。該藥是一款口服小分子生長激素促分泌劑,通過刺激垂體分泌內源性生長激素發揮治療作用。作為金賽藥業在生長激素領域的重點創新產品,GS3-007a以口服小分子促分泌劑的獨特定位,為生長激素缺乏相關疾病的治療與診斷提供了新路徑。其臨床開發的穩步推進,不僅有望解決現有治療方案中患者依從性不佳的痛點,更將推動國內生長激素治療市場的迭代升級。4項Ⅰ期臨床試驗中,有2項適應證為晚期實體瘤,試驗藥物分別為GenSci143和GenSci140。其中,GenSci143是全球首創的雙特異性ADC,靶向B7-H3與PSMA雙靶點,搭載TOPO-I抑制劑毒素,具有靶向化療和腫瘤免疫雙重治療效應,主要用于轉移性去勢抵抗性前列腺癌及其他B7-H3/ PSMA陽性晚期實體瘤治療。GenSci140是靶向葉酸受體α亞型(FRα)的雙表位ADC,采用可裂解連接子搭載TOPO-I抑制劑毒素,可同時結合FRα的不同表位,實現對中低表達FRα腫瘤的高效殺傷。其余2項Ⅰ期臨床試驗中,1項試驗藥物為GenSci142,適應證為細菌性陰道病(NCT07302035)。GenSci142是一款重組裂解酶類創新生物制品,靶向細菌性陰道病主要致病菌加德納菌,通過生物信息學技術從噬菌體序列中篩選并經人工智能優化獲得,可直接破壞細菌細胞壁使其快速裂解死亡,兼具精準殺菌、高效清除生物膜、低耐藥風險、保留陰道有益乳桿菌等核心優勢。另1項試驗藥物為GenSci098,適應證為Graves病(NCT07286656)。該藥是一款人源化抗促甲狀腺激素受體(TSHR)拮抗型單克隆抗體,采用長效制劑設計,可同時作用于甲狀腺和球后組織,阻斷致病性自身抗體與TSHR結合,從根源抑制甲亢和甲狀腺相關眼病的進展。
百利天恒2025年12月份新開的6項臨床試驗中,包含1項Ⅱ/Ⅲ期臨床、1項Ⅱ期臨床及4項Ⅰ期臨床。其中,Ⅱ/Ⅲ期臨床試驗的試驗藥物為BL-M11D1,適應證為急性髓性白血病(NCT07255872)。BL-M11D1是百利天恒與時邁藥業聯合開發的靶向CD33的ADC藥物,采用創新TOP1抑制劑Ed-04作為載荷,通過可切割連接子與CD33單抗偶聯,兼具抗體依賴的細胞毒性和靶向化療雙重作用。Ⅱ期臨床試驗的試驗藥物為BL-M07D1,適應證為非鱗狀非小細胞肺癌(NCT07264816)。BL-M07D1是百利天恒與時邁藥業聯合開發的靶向HER2的創新型ADC,以曲妥珠單抗為抗體骨架,通過組織蛋白酶B可切割連接子與新型TOP1抑制劑Ed-04偶聯而成。在4項Ⅰ期臨床試驗中,有2項試驗藥物均為BL-M24D1,適應證分別為頭頸部鱗狀細胞癌(NCT07232524)和多發性硬化癥(NCT07255898)。該藥是百利天恒自主研發的創新型ADC,采用MMAE/F類微管蛋白抑制劑作為載荷,具備高穩定性與高抗腫瘤活性。其余2項Ⅰ期臨床試驗中,有1項試驗藥物為放射性藥物镥[177Lu]-BL-ARC001,適應證為肺癌(NCT07274852)。該藥是百利天恒基于具有自主知識產權的HIRE-ARC平臺開發的全球首創抗體放射性核素偶聯藥物(ARC),通過高親和力抗體靶向遞送镥-177(177Lu)放射性核素發揮治療作用。最后1項Ⅰ期臨床試驗的試驗藥物為BL-M24D1,適應證為胃腸腫瘤(NCT07279428)。該藥同樣采用MMAE/F類微管蛋白抑制劑作為載荷,具備高穩定性與高抗腫瘤活性。
(數據來源于美國Clinicaltrial數據庫,統計時間為2026年1月10日)
《中國醫藥報》社版權所有,未經許可不得轉載使用。
(責任編輯:劉思慧)
右鍵點擊另存二維碼!
-
相關閱讀
-
為你推薦