每周醫(yī)藥看點(4月6日—12日)
- 2026-04-16 09:11
- 作者:
- 來源:中國食品藥品網(wǎng)
國務院印發(fā)《中國(內(nèi)蒙古)自由貿(mào)易試驗區(qū)總體方案》,明確增強服務貿(mào)易發(fā)展活力、培育口岸經(jīng)濟發(fā)展動力、增強醫(yī)藥產(chǎn)業(yè)發(fā)展動能等19個方面改革創(chuàng)新舉措,高標準高質(zhì)量建設(shè)中國(內(nèi)蒙古)自由貿(mào)易試驗區(qū);復方氯化鈉滴眼液、鹽酸氮卓斯汀滴眼液由處方藥轉(zhuǎn)換為非處方藥……4月6日—12日,醫(yī)藥行業(yè)的這些動態(tài)值得關(guān)注。
行業(yè)政策及藥監(jiān)動態(tài)
1.國務院印發(fā)《中國(內(nèi)蒙古)自由貿(mào)易試驗區(qū)總體方案》。方案明確了增強服務貿(mào)易發(fā)展活力、培育口岸經(jīng)濟發(fā)展動力、增強醫(yī)藥產(chǎn)業(yè)發(fā)展動能等19個方面改革創(chuàng)新舉措,著力打造聯(lián)通內(nèi)外、輻射周邊的信息交流中心、交通物流中心、要素資源配置中心、重點領(lǐng)域科技創(chuàng)新中心和產(chǎn)業(yè)合作中心,充分發(fā)揮國家向北開放重要橋頭堡作用,努力建成投資貿(mào)易便利、創(chuàng)新生態(tài)良好、優(yōu)勢產(chǎn)業(yè)集聚、國際交往活躍的高水平自由貿(mào)易園區(qū)。
2.國家藥監(jiān)局發(fā)布公告,決定將復方氯化鈉滴眼液、鹽酸氮卓斯汀滴眼液由處方藥轉(zhuǎn)換為非處方藥。品種名單及其非處方藥說明書范本一并發(fā)布。
3.國家藥監(jiān)局藥品審評中心(CDE)決定,將蘇州亞盛藥業(yè)有限公司的APG-115膠囊及海思科醫(yī)藥集團股份有限公司的HSK42360片納入兒童抗腫瘤藥物研發(fā)鼓勵試點計劃(星光計劃)。前者擬開發(fā)兒童適應證為神經(jīng)母細胞瘤、橫紋肌肉瘤、尤文肉瘤等實體瘤,后者擬開發(fā)兒童適應證為攜帶BRAF V600突變的復發(fā)或進展的腦膠質(zhì)瘤。
4.CDE發(fā)布《藥物上市申請臨床評價技術(shù)指導原則》,旨在更好地指導評價者對藥物上市申請中的臨床有效性、安全性及獲益-風險進行科學、規(guī)范且高效的評價,讓申請人了解臨床評價的關(guān)鍵考慮。該指導原則適用于化學藥品、治療用生物制品的藥物上市申請臨床專業(yè)評價工作,包括完整評價報告的結(jié)構(gòu)、內(nèi)容、方法和標準。
5.CDE發(fā)布《藥物臨床試驗申請臨床評價技術(shù)指導原則》,對藥物臨床試驗申請時臨床評價的關(guān)鍵技術(shù)考慮提出具體建議,供申請人、研究者和監(jiān)管機構(gòu)參考。該指導原則適用于化學藥品和治療用生物制品臨床試驗申請的評價。
6.CDE就《化學藥品創(chuàng)新藥分段生產(chǎn)藥學研究技術(shù)指導原則(征求意見稿)》公開征求意見。征求意見稿針對化學藥品創(chuàng)新藥生產(chǎn)中出現(xiàn)的分段生產(chǎn)的情形,明確相關(guān)研究技術(shù)要求,以更好地指導企業(yè)進行研究及統(tǒng)一技術(shù)審評尺度。
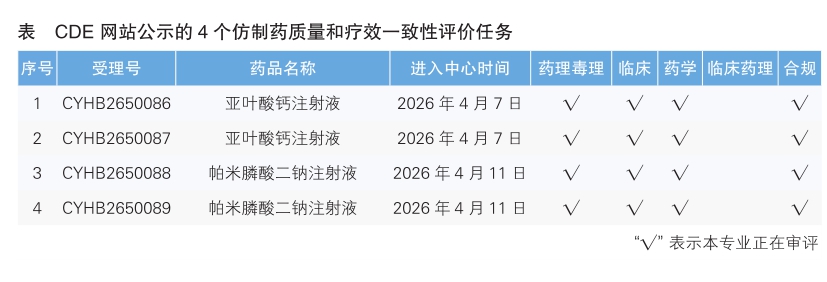
7.CDE網(wǎng)站公示4個仿制藥質(zhì)量和療效一致性評價任務(詳見表),涉及亞葉酸鈣注射液等品種。
產(chǎn)品研發(fā)上市信息
1.國家藥監(jiān)局發(fā)布3期藥品批準證明文件送達信息,共包括240個受理號,涉及北京匯恩蘭德制藥股份有限公司等企業(yè)。
2.CDE承辦受理52個新藥上市申請,包括HLX3902注射液等。
3.先聲再明宣布,其靶向CDH6的抗體偶聯(lián)藥物SIM0505獲美國食品藥品管理局(FDA)授予快速通道認定。
4.正大天晴宣布,公司研發(fā)的泛KRAS抑制劑TQB3205針對晚期惡性腫瘤的臨床試驗獲得美國FDA批準。
醫(yī)藥企業(yè)觀察
1.甘李藥業(yè)宣布,與韓國制藥企業(yè)JW Pharmaceutical簽署獨家許可協(xié)議,雙方就甘李藥業(yè)研發(fā)的胰高血糖素樣肽-1受體激動劑博凡格魯肽注射液在韓國的臨床開發(fā)、注冊申報及商業(yè)化開展合作。根據(jù)協(xié)議,JW Pharmaceutical將獲得在韓國開發(fā)和商業(yè)化博凡格魯肽注射液的獨家權(quán)益;甘李藥業(yè)將獲得一次性、不可退還首付款500萬美元,并可基于研發(fā)進展、監(jiān)管審批及商業(yè)化等情況,獲得總計7610萬美元的里程碑付款,以及產(chǎn)品商業(yè)化后根據(jù)凈銷售額收取的分級特許權(quán)使用費。
2.東阿阿膠宣布,與昂心生物達成項目合作。雙方將重點圍繞3個方面展開合作:利用昂心生物的人工智能藥物發(fā)現(xiàn)平臺加速生物醫(yī)藥研發(fā)進程;針對“卵巢早衰(POI)”研究項目進行深度合作;探討生物技術(shù)、人工智能與傳統(tǒng)中藥的融合。此次合作將推進東阿阿膠的復方阿膠漿在女性健康領(lǐng)域的科學基礎(chǔ)研究,助力傳統(tǒng)中藥與前沿科技實現(xiàn)跨界融合。
3.維健醫(yī)藥宣布,與雅各臣科研制藥簽署合作協(xié)議。維健醫(yī)藥將獲得雅各臣科研制藥三氧化二砷口服溶液在許可區(qū)域的獨家開發(fā)和商業(yè)化權(quán)益。
藥品集中采購
1.山西省藥械集中招標采購中心發(fā)布《關(guān)于做好34種藥品省際聯(lián)盟集中帶量采購品種數(shù)據(jù)填報工作的通知》,要求山西省各市醫(yī)保部門組織轄區(qū)內(nèi)相關(guān)醫(yī)藥機構(gòu),在規(guī)定時間內(nèi)完成采購需求量的填報工作。根據(jù)通知,此次藥品聯(lián)盟集中帶量采購產(chǎn)品包括特一藥業(yè)集團股份有限公司的紅霉素等。
2.上海市醫(yī)藥集中招標采購事務管理所發(fā)布《關(guān)于公布2026年1月藥品掛網(wǎng)公開議價采購監(jiān)管品種名單的通知》。根據(jù)通知,重慶天致藥業(yè)股份有限公司的利肺片等10個品種被納入重點監(jiān)控品種名單,上海普康藥業(yè)有限公司的寧心寶膠囊等10個品種被納入未通過公允性品種名單。通知要求,各醫(yī)療機構(gòu)根據(jù)市場供需情況以及陽光平臺“紅黃灰”標提醒信息,考慮臨床需求,采購質(zhì)量可靠、價格適宜的藥品。(劉鶴整理)
《中國醫(yī)藥報》社版權(quán)所有,未經(jīng)許可不得轉(zhuǎn)載使用。
(責任編輯:劉思慧)
右鍵點擊另存二維碼!
-
相關(guān)閱讀
-
為你推薦
互聯(lián)網(wǎng)新聞信息服務許可證10120170033
網(wǎng)絡出版服務許可證(京)字082號
?京公網(wǎng)安備 11010802023089號 京ICP備17013160號-1