每周醫藥看點(1月12日—18日)
- 2026-01-23 09:19
- 作者:
- 來源:中國醫藥報
國家藥監局發布《關于化學藥品和生物制品全面實施藥品電子通用技術文檔申報的公告》,加快推進藥品電子通用技術文檔(eCTD)在我國的實施進程;為配合eCTD全面實施,相關技術文件也進行了修訂……1月12日—18日,醫藥行業的這些動態值得關注。
行業政策及藥監動態
1.國家藥監局發布《關于化學藥品和生物制品全面實施藥品電子通用技術文檔申報的公告》,加快推進藥品eCTD在我國的實施進程。公告明確,自2026年3月1日起,化學藥品、化學原料藥和生物制品的藥物臨床試驗申請、藥品上市許可注冊申請、補充申請、境外生產藥品再注冊申請,以及仿制藥質量和療效一致性評價申請等,可按照eCTD方式申報。
2.國家醫保局就“藥品真實世界醫保綜合價值評價系列指南(試行)”公開征求意見,旨在加快建立全國統一的真實世界醫保綜合價值評價體系,為醫保目錄調整、支付標準確定、集采賦分等提供科學證據,促進醫保基金更合理使用。
3.國家藥監局藥品審評中心(CDE)發布通告,為配合eCTD的全面實施,CDE對eCTD V3.2.2相關技術文件進行了修訂。本次發布的技術文件包括《eCTD技術規范V1.1》《eCTD驗證標準V1.1》等,自2026年3月1日起施行。
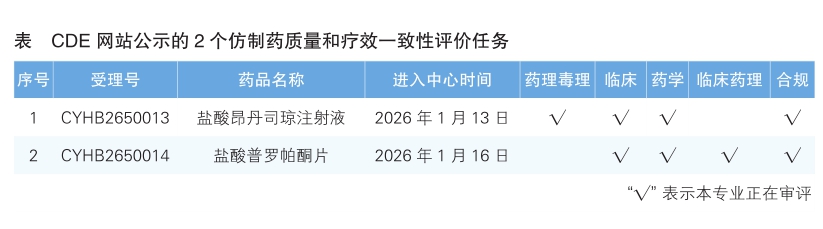
4.CDE網站公示2個仿制藥質量和療效一致性評價任務(詳見表),分別為鹽酸昂丹司瓊注射液和鹽酸普羅帕酮片。
5.國家中醫藥管理局綜合司發布《關于征集2026年度中醫藥標準制修訂項目建議的通知》。根據通知,此次標準制修訂項目主要涉及中醫藥基礎標準、中醫藥技術標準、中醫藥管理標準等。申報的項目建議應完成標準前期研制工作,形成相對成熟的標準草案,確保立項后18個月內(修訂項目12個月)能夠完成審查。
產品研發上市信息
1.國家藥監局發布4期藥品批準證明文件送達信息,共包括113個受理號,涉及華潤雙鶴藥業股份有限公司等企業。
2.CDE承辦受理64個新藥上市申請,包括溫膽湯顆粒等。
3.和譽醫藥宣布,其自主研發的新型口服高選擇性小分子集落刺激因子1受體(CSF-1R)抑制劑鹽酸匹米替尼膠囊用于腱鞘巨細胞瘤患者系統性治療的新藥申請(NDA),已獲美國食品藥品管理局(FDA)正式受理。
4.天澤云泰宣布,公司自主研發的用于治療戈謝病的AAV基因治療產品VGN-R08b獲得美國FDA授予的孤兒藥資格認定。
5.石藥集團宣布,集團開發的強效醛固酮合成酶抑制劑SYH2072片的臨床試驗申請已獲得美國FDA批準,適應證為未控制高血壓和難治性高血壓。
醫藥企業觀察
1.榮昌生物宣布,與艾伯維就榮昌生物自主研發的新型靶向PD-1/VEGF雙特異性抗體藥物RC148簽署獨家授權許可協議。根據協議,艾伯維將獲得RC148在許可區域的獨家開發、生產和商業化權利;榮昌生物將獲得6.5億美元首付款,并有資格獲得最高達49.5億美元的開發、監管和商業化里程碑付款,以及在許可區域凈銷售額的兩位數分級特許權使用費。
2.藥明生物宣布,與再鼎醫藥針對一款創新T細胞銜接子(TCE)簽署研究服務協議。根據協議條款,再鼎醫藥將獲得該TCE在實體瘤適應證治療上的全球獨家開發與商業化權利;藥明生物將獲得首付款,并有資格獲得開發、上市及銷售里程碑付款,以及產品上市后的銷售提成和再許可或其他BD交易付款。
3.復星凱瑞宣布,通過戰略合作獲得思比曼生物異體人源脂肪間充質干細胞注射液洛它阿托賽在許可區域的獨家商業化權益。洛它阿托賽是思比曼生物基于其異體間充質干細胞技術平臺開發的一款擁有自主知識產權的產品,旨在通過抑制炎癥并修復受損軟骨,為骨關節炎患者提供安全且長效的癥狀緩解,有望成為改變膝骨關節炎疾病進程的再生醫學產品。
4.金賽藥業宣布,與阿里健康達成戰略合作。雙方將在兒童健康成長、痛風防治、呼吸與過敏、女性健康、兒童神經與精神健康及營養補充六大板塊開展深度協同。金賽藥業將依托其在生物醫藥研發、臨床診療經驗等方面的核心競爭力,結合阿里健康在數據技術、平臺運營及用戶觸達方面的資源,共同探索“醫+藥+服務”一體化數字健康新模式。
藥品集中采購
1.四川省藥械招標采購服務中心發布通知稱,根據企業在四川省藥械集中采購及醫藥價格監管平臺提交的藥品降價申請,擬調低部分藥品的聯動參考價格,涉及成都天臺山制藥股份有限公司的阿侖膦酸鈉片等藥品。
2.海南省醫保局發布《關于做好廣東聯盟雙氯芬酸等批次采購中選結果執行工作的通知》,明確自3月1日起同步落地廣東聯盟雙氯芬酸、常見病慢性病藥品接續及京津冀“3+N”聯盟接續的中選結果,采購周期均為兩年。 (劉鶴整理)
《中國醫藥報》社版權所有,未經許可不得轉載使用。
(責任編輯:劉思慧)
右鍵點擊另存二維碼!
-
相關閱讀
-
為你推薦